ГЛИКОПИН инструкция по применению, состав, показания, противопоказания, побочные эффекты – таблетки
Гликопин® применяют животным перорально до кормления или во время кормления на корень языка или с водой для поения. Доза зависит от массы тела животного и цели применения.
В комплексной терапии и профилактике инфекционных болезней и комплексной терапии онкологических заболеваний - 0.04-0.06 мг/кг массы животного 1 раз/сут в течение 5-7 дней, из расчета:
| Вид и масса животного | Разовая доза препарата Гликопин®, таблетки |
| Собаки массой от 2 до 10 кг | 1/2-1 |
| Собаки массой более 10 кг | 1–2 |
| Кошки массой от 1 до 3 кг | 1/4-1/2 |
| Кошки массой более 3 кг | 1/2-1 |
| Декоративные грызуны, хорьки | 1/10* |
Для усиления эффективности вакцинации у ослабленных животных, профилактики поствакцинальных осложнений, повышения общей резистентности, стимуляции процессов репарации и регенерации тканей
 02-0.04 мг/кг массы животного однократно или двукратно с интервалом 24 ч, из расчета:
02-0.04 мг/кг массы животного однократно или двукратно с интервалом 24 ч, из расчета:| Вид и масса животного | Разовая доза препарата Гликопин®, таблетки |
| Собаки массой от 2 до 10 кг | 1/4-1/2 |
| Собаки массой более 10 кг | 1-11/2 |
| Кошки массой от 1 до 3 кг | 1/4 |
| Кошки массой более 3 кг | 1/2 |
| Декоративные грызуны, хорьки | 1/10* |
Для профилактики иммунодефицитов при стрессовых состояниях, иммунодефицитов новорожденных животных, сокращения периода инволюционных послеродовых процессов в матке - 0.01-0.02 мг/кг массы животного однократно или двукратно с интервалом 24 ч, из расчета:
| Вид животного | Разовая доза препарата Гликопин®, таблетки |
| Собаки | 1/2–1 |
| Кошки | 1/4-1/2 |
| Декоративные грызуны, хорьки | 1/10* |
* при применении препарата Гликопин® грызунам и хорькам 1 таблетку растворяют в 10 мл воды и вводят приготовленный раствор с помощью шприца в разовой дозе - 1 мл на животное.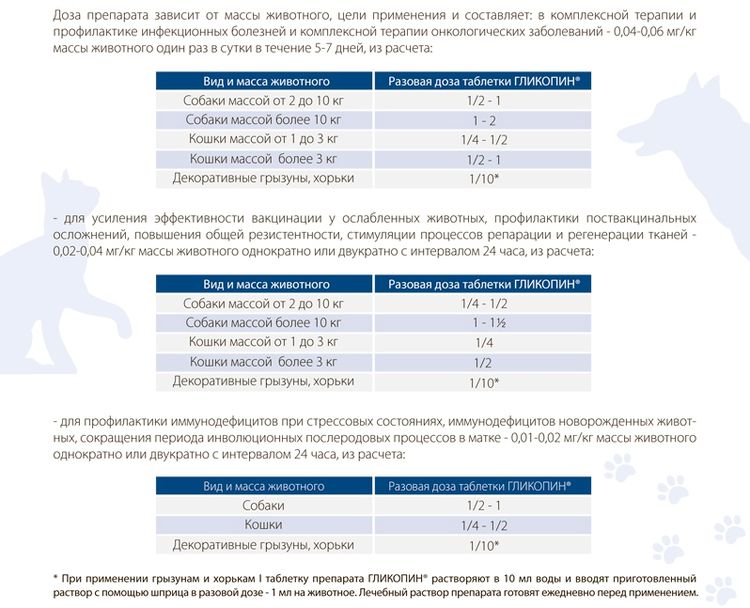 Лечебный раствор препарата готовят ежедневно перед применением.
Лечебный раствор препарата готовят ежедневно перед применением.
Особенностей действия препарата при его первом применении и отмене не установлено.
Следует избегать пропуска очередной дозы препарата, т.к. это может привести к снижению терапевтической эффективности. В случае пропуска одной дозы применение препарата возобновляют в той же дозе по той же схеме.
Гликопин® 1 мг | Собакам, кошкам, грызунам
В комплексной терапии и профилактике инфекционных болезней и комплексной терапии онкологических заболеваний – 0,04-0,06 мг/кг массы животного один раз в сутки в течение 5-7 дней, из расчета:
Вид и масса животного | Разовая доза Гликопин |
Декоративные грызуны, | 1/10* |
Для усиления эффективности вакцинации у ослабленных животных, профилактики поствакцинальных осложнений, повышения общей резистентности, стимуляции процессов репарации и регенерации тканей – 0,02–0,04 мг/кг массы животного однократно или двукратно с интервалом 24 часа, из расчета:
Вид и масса животного | Разовая доза Гликопин |
Декоративные грызуны, | 1/10* |
Для профилактики иммунодефицитов при стрессовых состояниях, иммунодефицитов новорожденных животных, сокращения периода инволюционных послеродовых процессов в матке – 0,01–0,02 мг/кг массы животного однократно или двукратно с интервалом 24 часа, из расчета:
Вид и масса животного | Разовая доза Гликопин |
Декоративные грызуны, | 1/10* |
*При применении грызунам и хорькам 1 таблетку препарата Гликопин® растворяют в 10 мл воды и вводят приготовленный раствор с помощью шприца в разовой дозе - 1 мл на животное.
Гликопин - инструкция по применению
Инструкция по применению лекарственного препарата Гликопин
(Организация - разработчик: ЗАО «Пептек», г. Москва)
I. Общие сведения
Торговое наименование лекарственного препарата: Гликопин.
Группировочное наименование: глюкозаминилмурамилдипептид.
Лекарственная форма: таблетки.
Действующее вещество: глюкозаминилмурамилдипептид (ГМДП) - 1 мг; вспомогательные вещества: лактозы моногидрат, сахароза, крахмал картофельный, метилцеллюлоза, кальция стеарат.
Гликопин по внешнему виду представляет собой круглые плоскоцилиндрические таблетки белого цвета с фаской.
Срок годности препарата при соблюдении условий хранения в закрытой упаковке - 5 лет со дня производства. Запрещается применение Гликопина по истечении срока годности.
Гликопин выпускают расфасованным по 10 таблеток в контурные ячейковые упаковки. По 1 контурной ячейковой упаковке вместе с инструкцией по применению помещают в картонную пачку.
По 1 контурной ячейковой упаковке вместе с инструкцией по применению помещают в картонную пачку.
Хранят препарат в закрытой упаковке производителя в сухом, защищённом от прямых солнечных лучей месте, отдельно от продуктов питания и кормов, при температуре от 0°С до 25°С в недоступном для детей месте.
Неиспользованный лекарственный препарат утилизируют в соответствии с требованиями законодательства.
Отпускают без рецепта ветеринарного врача.
II. Фармакологические (биологические) свойства
Гликопин относится к фармакотерапевтической группе: иммуномодулирующее средство.
Входящее в состав препарата Гликопин действующее вещество глюкозаминилмурамилдипептид (ГМДП) представляет собой минимальный фрагмент пептидогликана клеточной стенки бактерий. Биологическая активность ГМДП обусловлена взаимодействием со специфическим рецептором NOD2.
 Усиливая продукцию колониестимулирующих факторов, индуцирует лейкопоэз. В результате действия препарата происходит активация всех звеньев иммунной системы с усилением противоинфекционного и противоопухолевого иммунитета.
Усиливая продукцию колониестимулирующих факторов, индуцирует лейкопоэз. В результате действия препарата происходит активация всех звеньев иммунной системы с усилением противоинфекционного и противоопухолевого иммунитета. Гликопин после перорального введения быстро всасывается в кровь и достигает максимальной концентрации в плазме крови через 4 часа. Биодоступность составляет около 77%.
Большая часть введенного препарата метаболизируется полностью, 3-11% от введенной дозы препарата выводится с мочой, 19-21% - с фекалиями.
По степени воздействия на организм Гликопин относится к малоопасным веществам (4 класс опасности по ГОСТ 12.1 007-76), не оказывает местнораздражающего, тератогенного, эмбриотоксического, гепатотоксического и сенсибилизирующего действия.
III. Порядок применения
Гликопин применяют собакам, кошкам, декоративным грызунам и хорькам в комплексной терапии и профилактике инфекционных болезней бактериальной и вирусной этиологии; в комплексной терапии онкологических заболеваний; для повышения неспецифической резистентности организма молодняка и старых животных; усиления эффективности вакцинации у ослабленных животных с вторичным иммунодефицитом и уменьшения поствакцинальных осложнений, снятия стрессового состояния при транспортировке и различных зооветеринарных обработках, стимуляции процессов репарации и регенерации тканей после травм и оперативных вмешательств, для профилактики иммунодефицитов новорожденных животных, а также сокращения периода инволюционных послеродовых процессов в матке.
Противопоказанием для применения Гликопина является индивидуальная повышенная чувствительность животного к компонентам препарата.
Гликопин применяют животным перорально до кормления или во время кормления на корень языка или с водой для поения. Дозировка зависит от
массы тела животного и цели применения:
- в комплексной терапии и профилактике инфекционных болезней и комплексной терапии онкологических заболеваний - 0,04-0,06 мг/кг массы животного один раз в сутки в течение 5-7 дней, из расчета:
| Вид и масса животного | Разовая доза Гликопина, таблетки |
| Собаки массой от 2 до 10 кг | 1/2-1 |
| Собаки массой более 10 кг | 1-2 |
| Кошки массой от 1 до 3 кг | 1/4-1/2 |
| Кошки массой более 3 кг | 1/2-1 |
| Декоративные грызуны, хорьки | 1/10* |
- для усиления эффективности вакцинации у ослабленных животных, профилактики поствакцинальных осложнений, повышения общей резистентности, стимуляции процессов репарации и регенерации тканей - 0,02-0,04 мг/кг массы животного однократно или двукратно с интервалом 24 часа, из расчета:
| Вид и масса животного | Разовая доза Гликопина, таблетки |
| Собаки массой от 2 до 10 кг | 1/4-1/2 |
| Собаки массой более 10 кг | 1-11/2 |
| Кошки массой от 1 до 3 кг | 1/4 |
| Кошки массой более 3 кг | 1/2 |
| Декоративные грызуны, хорьки | 1/10* |
- для профилактики иммунодефицитов при стрессовых состояниях, иммунодефицитов новорожденных животных, сокращения периода инволюционных послеродовых процессов в матке - 0,01-0,02 мг/кг массы животного однократно или двукратно с интервалом 24 часа, из расчета:
| Вид и масса животного | Разовая доза Гликопина, таблетки |
| Собаки | 1/2-1 |
| Кошки | 1/4-1/2 |
| Декоративные грызуны, хорьки | 1/10* |
* При применении грызунам и хорькам 1 таблетку препарата Гликопин растворяют в 10 мл воды и вводят приготовленный раствор с помощью шприца в разовой дозе - 1 мл на животное. Лечебный раствор препарата готовят ежедневно перед применением.
Лечебный раствор препарата готовят ежедневно перед применением.
Симптомы передозировки при применении лекарственного препарата у животных не выявлены.
Особенностей действия препарата Гликопин при первом приеме и при его отмене не выявлено.
Беременность и лактация не являются противопоказанием для применения препарата, однако беременные животные должны принимать препарат под контролем ветеринарного врача. Возможно применение препарата у потомства животных, начиная с первых дней жизни.
Следует избегать пропуска очередной дозы препарата, так как это может привести к снижению терапевтической эффективности. В случае пропуска одной дозы, применение препарата возобновляют в той же дозе по той же схеме.
Побочных действий и нежелательных реакций при применении Гликопина в соответствии с настоящей инструкцией не отмечается. В отдельных случаях возможно незначительное и кратковременное повышение температуры тела животного, обусловленное фармакологическими свойствами препарата.
Лечение препаратом Гликопин не исключает применение антибактериальных препаратов.
Гликопин не рекомендуется применять одновременно с глюкокортикостероидными препаратами в высоких дозах. Препарат Гликопин возможно применять совместно с кормами. Случаи несовместимости препарата с другими препаратами и кормами не выявлены.
Лекарственный препарат Гликопин не предназначен для применения продуктивным животным.
IV. Меры личной профилактики
При применении препарата Гликопин следует соблюдать общие правила личной гигиены и техники безопасности, предусмотренные при работе с лекарственными препаратами.
После работы с препаратом следует вымыть руки с мылом.
При случайном попадании препарата в организм человека следует выпить несколько стаканов теплой воды, а при необходимости обратиться в медицинское учреждение, имея при себе картонную упаковку или инструкцию по применению препарата. Антидоты к препарату не требуются.
Наименования и адреса производственных площадок производителя лекарственного препарата для ветеринарного применения.
Наименование, адрес организации, уполномоченной держателем или владельцем регистрационного удостоверения лекарственного препарата на принятие претензий от потребителя: ЗАО «Пептек», Россия, 117997, г. Москва, ул. Миклухо-Маклая, 16/10.
Номер регистрационного удостоверения: 77-3-7.12-0689 № ПВР-З-3.9/00149
Гликопин - инструкция, описание, дозировка - Иммуномодуляторы, биостимуляторы
ГМДП (глюкозаминилмурамилдипептид) таблеткиРегистрационный номер ПВР -2-3.9 /00149
Гликопин повышает общую сопротивляемость организма животного к патогенному фактору, прежде всего за счет активации клеток фагоцитарной системы иммунитета (нейтрофилов и макрофагов).
Последние путем фагоцитоза уничтожают патогенные микроорганизмы и, в то же время, секретируют медиаторы естественного иммунитета - цитокины, которые, воздействуя на широкий спектр клеток-мишеней, вызывают дальнейшее развитие защитной реакции организма.
Препарат применяют для профилактики и лечения инфекционных заболеваний сельскохозяйственных и домашних животных; для снятия у них поствакцинальных осложнений и стрессового состояния.
Гликопин снижает частоту обострения при хронических заболеваниях, повышает эффективность антибактериальных и противовирусных препаратов.
Лечение Гликопином не исключает применение антибиотиков и других симптоматических средств, особенно у тяжелобольных животных.
Монотерапия Гликопином показана для животных с повышенной индивидуальной чувствительностью к другим лекарственным препаратам.
Препарат выпускается в форме таблеток, что упрощает его применение в амбулаторной практике.
Таблетки и порошок слегка сладковатые на вкус хорошо поедаются всеми животными.
Побочных явлений и осложнений при применении Гликопина не отмечается.
Противопоказаний не установлено.
Известен молекулярный механизм действия.
КЛИНИЧЕСКОЕ ПРИМЕНЕНИЕ ГЛИКОПИНА
Птица
Инфекционные заболевания вирусной и бактериальной этиологии
При лечении инфекционных заболеваний вирусной и бактериальной этиологии молодняку домашней птицы в возрасте 1-20 дней, назначают Гликопин в виде кормовой добавки в дозе 0,03 мг/кг живой массы один раз в сутки в течение 5-7 дней, в зависимости от тяжести болезни.
Кошки
Инфекционные заболевания вирусной и бактериальной этиологии, заживление послеоперационных и гнойно-некротических ран:
При лечении инфекционных заболеваний вирусной и бактериальной этиологии кошкам назначают Гликопин внутрь в дозе 0,10-0,15 мг/кг один раз в сутки в течение 5-7 дней, в зависимости от тяжести болезни (кошкам с живым весом до 3 кг - 0,5-1 таблетки в день,
выше 3 кг - 1-2 таблетки в день).
Повышение общей резистентности и профилактика поствакцинальных осложнений:
Для повышения общей резистентности беременных самок и их приплода, сокращения периода инволюционных послеродовых процессов в матке, а также, для профилактики поствакцинальных осложнений Гликопин применяют внутрь в дозе 0,05-0,08 мг/кг массы животных 1-2 кратно с интервалом 24 часа (кошкам с живым весом до 3 кг - 0,25-0,5 таблетки в день, выше 3 кг - 0,5-1 таблетки в день).
Профилактика снижения иммунитета при стрессовых состояниях:
Для профилактики снижения иммунитета при стрессовых состояниях, вызываемых участием в выставках, транспортировкой, стрижкой и различными обработками, животным назначают Гликопин внутрь (внутримышечно или перорально) в дозе 0,03-0,05 мг/кг живой массы однократно за 1-2 дня до предполагаемых мероприятий (кошкам 0,25-0,5 таблетки в день).
Собаки
Инфекционные заболевания вирусной и бактериальной этиологии, заживление послеоперационных и гнойно-некротических ран:
При лечении инфекционных заболеваний вирусной и бактериальной этиологии, а также для заживления послеоперационных и гнойно-некротических ран собакам назначают Гликопин внутрь (перорально) в дозе 0,10-0,15 мг/кг один раз в сутки в течение 5-7 дней, в зависимости от тяжести болезни (собакам с живым весом до 10 кг - 0,5-2 таблетки, выше 10 кг - 2-4 таблетки в день).
Повышение общей резистентности и профилактика поствакцинальных осложнений.
Для повышения общей резистентности беременных самок и их приплода, сокращения периода инволюционных послеродовых процессов в матке, а также, для профилактики поствакцинальных осложнений Гликопин применяют внутрь (перорально) в дозе 0,05-0,08 мг/кг массы животных 1-2 кратно с интервалом 24 часа (собакам с живым весом до 10 кг - 0,25-1 таблетки, выше 10 кг - 1-2 таблетки в день).
Профилактика снижения иммунитета при стрессовых состояниях:
Для профилактики снижения иммунитета при стрессовых состояниях, вызываемых участием в выставках, транспортировкой, стрижкой и различными обработками, животным назначают Гликопин внутрь (перорально) в дозе 0,03-0,05 мг/кг живой массы однократно за 1-2 дня до предполагаемых мероприятий (собакам с живым весом до 10 кг - 0,5-1 таблетки, выше 10 кг - 2-4 таблетки в день).
Супертёплый дом-термос для Вашей собаки!
Гликопин — инструкция по применению иммуномодулятора
Ветеринарные препараты
Препарат выпускает французская фирма Virbac. Действующие компоненты — перметрин, фипронил. Терапевтическая форма — раствор для наружного
Действующие компоненты — перметрин, фипронил. Терапевтическая форма — раствор для наружного
Ветеринарные препараты
Биопрепараты выпускает французская компания Merial. Терапевтическая форма — лиофилизированная таблетка и растворитель. Вакцины фасуют во
Ветеринарные препараты
Препарат выпускает чешская компания Bioveta, a. s. Активный компонент — клопростенол, зарегистрирован ВОЗ. Лекарственная форма — раствор
s. Активный компонент — клопростенол, зарегистрирован ВОЗ. Лекарственная форма — раствор
Ветеринарные препараты
Препарат изготавливает белорусское предприятие «Белэкотехника». Активные компоненты — тилозин, сульфадимидин, колистин, триметоприм. Терапевтическая форма — порошок
Ветеринарные препараты
Лекарственное средство изготавливает российская компания Apicenna («Апи-Сан»). Действующий компонент — эприномектин. Терапевтическая форма — раствор для
Действующий компонент — эприномектин. Терапевтическая форма — раствор для
Ветеринарные препараты
Препарат изготавливает российская фирма «Ветзвероцентр». Действующее вещество — альфациперметрин. Терапевтическая форма — эмульсия для наружного применения.
Новое. Косметика, лекарства на интернет-аукционе Au.ru
Гликопин — лекарственное средство в форме таблеток, содержащее в своем составе в качестве действующего вещества N-ацетилглюкозаминил-N-ацетилмурамоил-аланил-D-изоглутамин (ГМДП) — 1 мг в 1 таблетке, а в качестве вспомогательных компонентов: сахар молочный, сахар или сахарозу, крахмал картофельный, метилцеллюлозу марки МЦ-100 и кальция стеарат.
Гликопин представляет собой круглые таблетки без оболочки белого цвета слегка сладковатого вкуса, массой 0,1 г.
Гликопин выпускают в пачках картонных, содержащих 1 ячейковую контурную упаковку из 10 таблеток. Каждую ячейковую контурную упаковку маркируют с указанием организации производителя и товарного знака, названия лекарственного средства, количества действующего вещества в таблетке, количества таблеток, номера серии и срока годности. Каждую пачку маркируют с указанием организации производителя, ее адреса и товарного знака, названия лекарственного средства, количества действующего вещества в таблетке, номера серии, даты изготовления, срока годности, количества таблеток в упаковке, надписи «Для животных», условий хранения, обозначения технических условий и снабжают инструкцией по применению. Гликопин хранят в упаковке организации-производителя в сухом, защищенном от света месте при температуре от 0 до 25 ºС. Срок годности препарата при соблюдении условий хранения — 5 лет со дня изготовления. Гликопин по истечении срока годности не должен применяться.
Гликопин по истечении срока годности не должен применяться.
II. ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Гликопин представляет собой основную структурную единицу пептидогликана клеточной стенки бактерий. Воздействует на клетки врожденной иммунной системы, связываясь со специфическим рецептором NOD2. Вызывает стимуляцию эффекторных функций фагоцитов (фагоцитоз, синтез активных форм кислорода, активность лизосомальных ферментов, презентация антигенов) и продукцию провоспалительных цитокинов, в свою очередь, индуцирующих пролиферацию, активацию и дифференцировку клеток приобретенного иммунитета — Т- и В-лимфоцитов. Через усиление продукции колониестимулирующих факторов индуцирует лейкопоэз. В результате действия препарата происходит активация всех звеньев иммунной системы с усилением противоинфекционного и противоопухолевого иммунитета.
После перорального введения быстро всасывается в кровь. Максимальная концентрация в плазме неизменного ГМДП выявляется через 4 часа. Биодоступность составляет около 77%. Полностью метаболизируется через 8 часов. Продукты метаболизма обнаруживаются в кровотоке в течение 12 часов и выводятся, главным образом, через почки с мочой. По степени воздействия на организм Гликопин относится к малоопасным веществам (4 класс опасности по ГОСТ 12.1 007-76). Препарат не обладает тератогенным и мутагенным эффектом. Не оказывает местнораздражающего и сенсибилизирующего действия.
Полностью метаболизируется через 8 часов. Продукты метаболизма обнаруживаются в кровотоке в течение 12 часов и выводятся, главным образом, через почки с мочой. По степени воздействия на организм Гликопин относится к малоопасным веществам (4 класс опасности по ГОСТ 12.1 007-76). Препарат не обладает тератогенным и мутагенным эффектом. Не оказывает местнораздражающего и сенсибилизирующего действия.
III. ПОРЯДОК ПРИМЕНЕНИЯ
Гликопин применяют в комплексе лечения и профилактики инфекционных болезней бактериальной и вирусной этиологии, для повышения общей резистентности организма молодняка и старых животных, для усиления эффективности вакцинации у ослабленных животных с вторичным иммунодефицитом, уменьшения поствакцинальных осложнений, для снятия стрессового состояния у животных при транспортировке и различных зооветеринарных обработках, для стимуляции процессов репарации и регенерации тканей после травм и оперативных вмешательств, для профилактики иммунопатологии у потомства беременных самок, сокращения периода инволюционных послеродовых процессов в матке. Гликопин применяют внутрь до или во время кормления.
Гликопин применяют внутрь до или во время кормления.
В комплексе лечения и профилактики инфекционных болезней бактериальной и вирусной этиологии животным назначают Гликопин в дозе 0,04-0,06 мг/кг один раз в сутки в течение 5-7 дней, в зависимости от тяжести болезни (собакам массой до 10 кг — 0,5-1 таблетку, выше 10 кг — 1-2 таблетки; кошкам массой до 3 кг — 0,25-0,5 таблетки, выше 3 кг — 0,5-1 таблетку).
Информация носит исключительно информационный характер. Перед применением препарата необходимо проконсультироваться с ветеринарным специалистом.
Таблетки «Гликопин» для кошек: отзывы, инструкция по применению
Как известно, кошки обладают от природы довольно сильным иммунитетом. Но в результате плохого питания, а также контакта с инфицированными животными здоровый питомец может быть подвернут риску получения опасных заболеваний. Препарат «Гликопин» для кошек, отзывы о котором вы можете прочитать в данной статье, считается отличным иммуномодулятором, очень часто назначаемым ветеринарами.
Используя данное средство для здорового животного, вы максимально повышаете его иммунитет, а если ваш любимый котик уже заболел, то данный медицинский препарат ускорит процесс его выздоровления в несколько раз.
Форма выпуска
Препарат «Гликопин» для кошек, отзывы о котором вы можете прочитать в данной статье, выпускается в виде таблеток, находящихся в блистерах, по десять штук в каждом. Пластинка с таблетками обычно помещается в картонную упаковку. Препарат обладает довольно приятным сладким вкусом, поэтому не придется насильно заставлять ваше животное его принимать.
Особенности действия
При поступлении в организм активные вещества всасываются очень быстро. Уже через четыре часа иммунитет животного значительно повышается. Таблетки обладают противовоспалительным, противоинфекционным и противоопухолевым действием. После применения препарата клетки насытятся кислородом, а также приступят к работе лизосомальные ферменты, уничтожающие огромное количество чужеродных тел. В это же время активизируются все иммунные процессы организма. Большая часть продуктов распада выводится из организма через почки.
В это же время активизируются все иммунные процессы организма. Большая часть продуктов распада выводится из организма через почки.
В каких случаях назначают препарат
«Гликопин» для кошек, отзывы о котором в большей степени положительные, назначают, в первую очередь, для устранения иммунодефицита. Также препарат оправдывает себя при сильнейших отравлениях животного, так как повышает сопротивляемость организма к опасным инфекциям.
Ветеринары рекомендуют использовать препарат «Гликопин» для кошек, отзывы о котором описаны в этой статье, в таких случаях:
- при попадании в организм инфекций;
- при наличии загноившихся ран с признаками некроза тканей;
- если у животного имеются доброкачественные опухоли;
- после перенесенной хирургической операции;
- для повышения общего иммунитета животного;
- при септическом шоке.
Используя препарат в качестве профилактики, вы убережете вашего домашнего питомца от многих заболеваний.
Несколько слов о назначении
Более подвержены заболеваниям кошки, проживающие на частных территориях. У них иммунитет более ослаблен из-за плохих погодных условий, а также из-за холодной и дождливой погоды. «Гликопин» – таблетки для кошек и собак, которые являются отличным средством для борьбы с сезонными простудами ваших любимцев.
У них иммунитет более ослаблен из-за плохих погодных условий, а также из-за холодной и дождливой погоды. «Гликопин» – таблетки для кошек и собак, которые являются отличным средством для борьбы с сезонными простудами ваших любимцев.
Препарат придет на помощь также и раненым животным. Поврежденные участки начнут быстрее заживать и рубцеваться. При этом вы заметите, как улучшится шерсть вашего любимца. Она станет гладкой и блестящей, пропадут все грибковые заболевания. Специалисты рекомендуют давать животному средство перед вязкой. Это увеличивает шансы на рождение здоровых котят и щенят.
Инструкция по использованию препарата
Чтобы лекарство дало нужный эффект, а также не нанесло вреда вашему домашнему питомцу, используйте его, точно опираясь на инструкцию по применению. Если животное не может самостоятельно употребить таблетку, тогда придется это сделать принудительно. Ее можно добавить в любимый корм вашего питомца или же положить ее ему под язык. Оба способа будут одинаково эффективными.
Подбор правильной дозировки
Препарат «Гликопин» (Glikopin), описание которого вы можете прочитать в этой статье, должен быть использован в правильной дозировке. От этого зависит его эффективность и безопасность.
Дозировка определяется в соответствии с массой животного, а также с основной целью использования. Для маленьких котят весом до двух килограмм будет достаточно четвертой части таблетки для лечения, и восьмой – для профилактики. Котам до трех килограмм подходит дозировка от четверти до половины пилюли. А взрослым котам весом более трех килограмм дают обычно целую таблетку или ее половинку.
Для эффективности лечения животное должно принимать лекарство один раз в день на протяжении недели. В некоторых случаях срок может быть увеличен или, наоборот, уменьшен. Все подробности лечения вам расскажет опытный ветеринар.
Существуют ли противопоказания
Вот такое имеет препарат «Гликопин» описание. Отзывы владельцев животных говорят о том, что данное лекарственное средство является нетоксичным, поэтому оно безопасно для использования в домашних условиях. Однако стоит учитывать, что вещества, входящие в его состав, могут вызывать аллергические реакции. Также ветеринары не рекомендуют принимать параллельно другие препараты без предварительной консультации, иначе вы можете нанести непоправимый вред животному.
Однако стоит учитывать, что вещества, входящие в его состав, могут вызывать аллергические реакции. Также ветеринары не рекомендуют принимать параллельно другие препараты без предварительной консультации, иначе вы можете нанести непоправимый вред животному.
Отзывы
На «Гликопин» обращают внимание не только хозяева взрослых кошек, но и владельцы маленьких котят. Многие люди пользуются советами ветеринаров и применяют данные таблетки как профилактическое средство. После его использования даже кошки, проводящие много времени на улице, не заражаются инфекционными заболеваниями и простудами.
В Интернете можно встретить много положительных отзывов о средстве, используемом для лечения пушистых любимцев. Хозяева животных сообщают, что их питомцы очень быстро крепнут, у них появляется жизненный тонус, улучшается аппетит, нормализуется стул, и болезнь проходит. Однако некоторые владельцы котов замечали и нежелательные эффекты после применения препарата, которые проявлялись в виде рвоты и поноса.
Таблетки «Гликопин»: отзывы врачей
Очень часто ветеринары рекомендуют применять лекарственный препарат «Гликопин» хозяевам домашних животных. Средство действительно очень эффективное, проверенное и надежное. Рекомендуется давать данные таблетки котятам, найденным на улице, а также домашним котам в профилактических целях. Описано много случаев, когда препарат «Гликопин» спасал жизнь животным. Являясь очень эффективным иммуномодулятором, он значительно повышает защитные силы организма, поэтому процесс выздоровления протекает намного быстрее.
Ветеринары советуют владельцам домашних питомцев применять это средство после перенесенных операций. Активные компоненты медикамента поспособствуют быстрому восстановлению вашего любимца. Если вы заботитесь о здоровье котенка или взрослого кота, не проходите мимо этих таблеток. С их помощью вы будете иметь сильное, жизнерадостное и счастливое животное. Не запускайте болезни, лучше проведите профилактические мероприятия. Каждый ветеринар вам скажет о том, что любое заболевание легче предупредить, чем лечить.
Применение, преимущества и побочные эффекты ликопина
- Натуральные продукты (Потребительские)
- Ликопин
Проверено с медицинской точки зрения Drugs.com. Последнее обновление 5 октября 2020 г.
Какие еще распространенные имена?
- Пси-каротин
- фунтов на квадратный дюйм
- All-Trans Ликопин
- Ликопены
- Ликопено
- Пси-пси-каротин
Для чего используется этот продукт?
Ликопин используется некоторыми людьми для предотвращения рака или сердечных заболеваний.Другие считают, что это поможет при диабете.
Какие меры предосторожности при приеме этого продукта?
Прежде чем использовать натуральный продукт, обязательно посоветуйтесь с врачом.
 Некоторые продукты могут плохо смешиваться с лекарствами или другими натуральными продуктами.
Некоторые продукты могут плохо смешиваться с лекарствами или другими натуральными продуктами.Этот продукт может мешать проведению некоторых лабораторных тестов. Обязательно поговорите со своим врачом об этом и обо всех лекарствах, которые вы принимаете.
Будьте особенно внимательны и проконсультируйтесь с врачом, если у вас рак.
На что смотреть?
Расстройство желудка
Спазмы желудка
Изжога
Когда мне нужно вызывать врача?
Признаки очень плохой реакции. К ним относятся хрипы; стеснение в груди; высокая температура; зуд; сильный кашель; голубой цвет кожи; судороги; или отек лица, губ, языка или горла.
 Немедленно сходите в скорую.
Немедленно сходите в скорую.Очень сильная рвота
Очень сильная боль в животе
Очень плохой жидкий стул
Дата последнего пересмотра
2016-12-06
Использование информации для потребителей
Эта информация не является конкретной медицинской консультацией и не заменяет информацию, которую вы получаете от своего поставщика медицинских услуг.Только ваш лечащий врач обладает знаниями и подготовкой, чтобы дать совет, который подходит вам. Вы не должны полагаться на эту информацию при принятии решения о том, следует ли использовать или принимать рекомендации вашего лечащего врача относительно использования любых натуральных продуктов или аналогичных методов лечения, терапии или выбора образа жизни. Эта информация не подтверждает, что какие-либо натуральные продукты или аналогичные методы лечения, методы лечения или образ жизни безопасны, эффективны или одобрены для лечения любого пациента или состояния здоровья. Это лишь краткое изложение общей информации. Он НЕ включает всю информацию о натуральных продуктах, возможном использовании, направлениях, предупреждениях, мерах предосторожности, взаимодействиях, побочных эффектах или рисках, которые могут относиться к вам. Вы должны поговорить со своим лечащим врачом для получения полной информации о вашем здоровье и вариантах лечения.
Это лишь краткое изложение общей информации. Он НЕ включает всю информацию о натуральных продуктах, возможном использовании, направлениях, предупреждениях, мерах предосторожности, взаимодействиях, побочных эффектах или рисках, которые могут относиться к вам. Вы должны поговорить со своим лечащим врачом для получения полной информации о вашем здоровье и вариантах лечения.
Авторское право
Авторское право © 2018 Wolters Kluwer Clinical Drug Information, Inc. и ее аффилированные лица и / или лицензиары. Все права защищены.
Подробнее о ликопине
Профессиональные ресурсы
Сопутствующие лечебные руководства
Дополнительная информация
Всегда консультируйтесь со своим врачом, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об отказе от ответственности
Таблетки «Гликопин» для кошек: отзывы, инструкция по применению - Лекарственные препараты
.
Как известно, у кошек от природы довольно сильный иммунитет. Но в результате неправильного питания, а также контакта с инфицированными животными здоровый питомец может оказаться в группе риска заразиться опасными заболеваниями. Препарат «Гликопин» для кошек, отзывы о котором вы можете прочитать в этой статье, считается отличным иммуномодулятором, очень часто назначается ветеринарами.
Применив это средство для здорового животного, вы максимально повысите его иммунитет, а если любимая кошка уже заболела, то этот лечебный препарат ускорит ее выздоровление в несколько раз.
Форма выпуска
Препарат «Гликопин» для кошек, отзывы о котором вы можете прочитать в этой статье, выпускается в форме таблеток, которые находятся в блистерах по десять штук в каждой. Таблетка обычно помещается в картонную коробку. Препарат имеет довольно приятный сладковатый вкус, поэтому заставлять животное его принимать не придется.
Особенности действия
При попадании в организм активные вещества очень быстро всасываются. Через четыре часа иммунитет животного значительно повышается.Таблетки обладают противовоспалительным, противоинфекционным и противоопухолевым действием. После применения препарата клетки насыщаются кислородом, и лизосомальные ферменты начинают работать, уничтожая огромное количество инородных тел. При этом активизируются все иммунные процессы в организме. Большая часть продуктов распада выводится через почки.
Через четыре часа иммунитет животного значительно повышается.Таблетки обладают противовоспалительным, противоинфекционным и противоопухолевым действием. После применения препарата клетки насыщаются кислородом, и лизосомальные ферменты начинают работать, уничтожая огромное количество инородных тел. При этом активизируются все иммунные процессы в организме. Большая часть продуктов распада выводится через почки.
В каких случаях назначают препарат
«Гликопин» для кошек, отзывы о котором в основном положительные, назначают, в первую очередь, для устранения иммунодефицита.Также препарат оправдывает себя при тяжелых отравлениях животных, так как повышает сопротивляемость организма опасным инфекциям.
Ветеринары рекомендуют применять препарат «Гликопин» кошкам, отзывы о которых описаны в данной статье, в таких случаях:
- при попадании инфекции внутрь;
- при наличии нагноившихся ран с признаками некроза тканей;
- , если у животного доброкачественные опухоли;
- после операции;
- для повышения общего иммунитета животного;
- с септическим шоком.

Применяя препарат в качестве профилактики, вы убережете своего питомца от многих болезней.
Несколько слов о записи
Более восприимчивы к кошкам, живущим на частных территориях. Их иммунитет более ослаблен из-за плохих погодных условий, а также холода и дождя. «Гликопин» - таблетки для кошек и собак, которые являются прекрасным средством борьбы с сезонными холодами ваших питомцев.
Препарат придет на помощь и раненым животным. Поврежденные участки начнут заживать быстрее.В то же время вы заметите, как улучшается шерсть вашего питомца. Он станет гладким и блестящим, исчезнут все грибковые заболевания. Специалисты рекомендуют давать животному средство перед вязкой. Это увеличивает шансы на появление здоровых котят и щенков.
Инструкция по применению препарата
Чтобы лекарство оказало желаемый эффект, а также не навредило вашему питомцу, применяйте его, точно полагаясь на инструкцию по применению. Если животное не может использовать таблетку самостоятельно, то его придется принудить. Его можно добавить в любимую еду вашего питомца или положить ему под язык. Оба метода будут одинаково эффективны.
Его можно добавить в любимую еду вашего питомца или положить ему под язык. Оба метода будут одинаково эффективны.
Подбор правильной дозировки
Препарат Гликопин (Glikopin), описание которого вы можете прочитать в этой статье, следует применять в правильной дозировке. От этого зависит его эффективность и безопасность.
Дозировка определяется в соответствии с массой животного, а также с основной целью использования. Маленьким котятам весом до двух килограммов хватит четвертой таблетки для лечения, а восьмой - для профилактики.Кошкам до трех килограммов подойдет дозировка от четверти до половины таблетки. А взрослым кошкам с массой тела более трех килограммов обычно дают целую таблетку или половину ее.
Чтобы быть эффективным, животное должно принимать лекарство один раз в день в течение недели. В некоторых случаях срок может быть продлен или, наоборот, сокращен. Все подробности лечения вам расскажет опытный ветеринарный врач.
Есть ли противопоказания?
А вот и описание препарата «Гликопин». Отзывы владельцев домашних животных говорят о том, что препарат нетоксичен, поэтому его безопасно использовать в домашних условиях. Однако следует учитывать, что входящие в его состав вещества могут вызывать аллергические реакции. Также ветеринары не рекомендуют принимать параллельно другие препараты без предварительной консультации, иначе можно нанести животному непоправимый вред.
Отзывы владельцев домашних животных говорят о том, что препарат нетоксичен, поэтому его безопасно использовать в домашних условиях. Однако следует учитывать, что входящие в его состав вещества могут вызывать аллергические реакции. Также ветеринары не рекомендуют принимать параллельно другие препараты без предварительной консультации, иначе можно нанести животному непоправимый вред.
Отзывы
На Гликопин обращают внимание не только владельцы взрослых кошек, но и владельцы маленьких котят. Многие пользуются советами ветеринаров и используют эти таблетки в качестве профилактического средства.После его использования даже кошки, которые много времени проводят на улице, не заражаются инфекционными заболеваниями и простудными заболеваниями.
В Интернете можно найти множество положительных отзывов об средстве, применяемом для лечения пушистых питомцев. Хозяева животных сообщают, что их питомцы очень быстро становятся сильнее, у них появляется жизненный тонус, улучшается аппетит, нормализуется стул, и болезнь проходит. Однако некоторые владельцы кошек также заметили нежелательные эффекты после применения препарата, которые проявлялись в виде рвоты и диареи.
Однако некоторые владельцы кошек также заметили нежелательные эффекты после применения препарата, которые проявлялись в виде рвоты и диареи.
Таблетки «Гликопин»: отзывы врачей
Очень часто ветеринары рекомендуют применять препарат «Гликопин» владельцам домашних животных. Средство действительно очень эффективное, проверенное и надежное. Эти таблетки рекомендуется давать котятам, найденным на улице, а также домашним кошкам в профилактических целях. Описано множество случаев, когда препарат «Гликопин» спасал жизни животных. Являясь очень эффективным иммуномодулятором, он значительно повышает защитные силы организма, поэтому процесс заживления протекает намного быстрее.
Ветеринары советуют владельцам домашних животных пользоваться этим средством после операции. Активные компоненты препарата поспособствуют скорейшему выздоровлению вашего питомца. Если вы заботитесь о здоровье котенка или взрослой кошки, не проходите мимо этих таблеток. С ними у вас будет крепкое, веселое и счастливое животное. Не запускайте болезнь, лучше проведите профилактические мероприятия. Каждый ветеринар скажет вам, что любое заболевание легче предотвратить, чем вылечить.
Не запускайте болезнь, лучше проведите профилактические мероприятия. Каждый ветеринар скажет вам, что любое заболевание легче предотвратить, чем вылечить.
GlucaGen® HypoKit®, инструкция по применению
Для получения полной информации см. Инструкцию по эксплуатации, прилагаемую к вашему GlucaGen ® HypoKit ® .
Приготовление дозы GlucaGen
® : Лекарство GlucaGen ® выпускается в виде сухого порошка. Перед использованием GlucaGen ® необходимо смешать сухой порошок со шприцем со стерильной водой, входящей в состав GlucaGen ® HypoKit ® . Не используйте другие жидкости для смешивания лекарства. Убедитесь, что оранжевая пластиковая крышка на флаконе с GlucaGen ® плотно закрыта. Не используйте флакон с GlucaGen ® , если оранжевый пластиковый колпачок ослаблен или отсутствует.
Не используйте флакон с GlucaGen ® , если оранжевый пластиковый колпачок ослаблен или отсутствует.
Шаг 1. Большим пальцем снимите оранжевую пластиковую крышку с флакона GlucaGen ® .
Шаг 2. Возьмите предварительно заполненный шприц со стерильной водой. Удерживая шприц одной рукой, другой рукой снимите крышку иглы со шприца. Не снимайте пластиковый ограничитель обратного хода со шприца.
Удерживая шприц одной рукой, другой рукой снимите крышку иглы со шприца. Не снимайте пластиковый ограничитель обратного хода со шприца.
Шаг 3. Возьмите флакон с GlucaGen ® . Удерживая флакон с сухим порошком одной рукой, другой рукой протолкните иглу предварительно заполненного шприца через центр резиновой пробки.
Шаг 4. Удерживайте флакон и шприц вместе, при этом игла все еще находится во флаконе. Осторожно переверните флакон и шприц лицевой стороной вверх. Медленно опускайте поршень вниз, пока шприц не опустеет. Не вынимайте шприц из флакона.
Удерживайте флакон и шприц вместе, при этом игла все еще находится во флаконе. Осторожно переверните флакон и шприц лицевой стороной вверх. Медленно опускайте поршень вниз, пока шприц не опустеет. Не вынимайте шприц из флакона.
Шаг 5. Возьмите все устройство (флакон и шприц) в одну руку и осторожно встряхните флакон до полного растворения порошка. Не используйте, если образовался гель или если вы видите частицы в растворе. Не вынимайте шприц из флакона.
Шаг 6. Крепко удерживайте флакон и шприц вместе, при этом игла все еще находится во флаконе. Осторожно переверните флакон и шприц вверх дном. Осторожно потяните за поршень и медленно наберите всю жидкость в шприц. Не вытягивайте поршень из шприца.
Крепко удерживайте флакон и шприц вместе, при этом игла все еще находится во флаконе. Осторожно переверните флакон и шприц вверх дном. Осторожно потяните за поршень и медленно наберите всю жидкость в шприц. Не вытягивайте поршень из шприца.
Шаг 7. Держите иглу во флаконе. Проверьте шприц на наличие пузырьков воздуха. Если вы видите пузырьки, нажимайте на шприц, пока пузырьки не поднимутся на верхушку шприца. Слегка надавите на поршень, чтобы вернуть во флакон только пузырьки воздуха.
Шаг 8. Держите флакон и шприц, как показано.
Держите флакон и шприц, как показано.
- Обычная доза для взрослых и детей, вес которых превышает 55 фунтов (25 кг), составляет 1 мг (1 мл). Используйте содержимое полного шприца (1 мл).
- Обычная доза для детей с массой тела менее 55 фунтов (25 кг) составляет 0,5 мг (0,5 мл). Осторожно нажмите на поршень, пока он не окажется в положении 0.Отметка 5 мл на шприце, чтобы убедиться, что в шприце осталось 0,5 мл жидкости.
Выньте шприц и иглу из флакона, когда в шприце будет правильная доза GlucaGen ® .
Если вы не знаете, сколько весит ребенок:
- Дайте ребенку до 6 лет 0,5 мг (0,5 мл).
- Дайте детям от 6 лет и старше 1 мг (1 мл).
Введение инъекции GlucaGen
® : Шаг 9. Выберите место инъекции. Обычные места инъекции GlucaGen ® - это плечи, бедра или ягодицы.
Выберите место инъекции. Обычные места инъекции GlucaGen ® - это плечи, бедра или ягодицы.
Шаг 10. Одной рукой осторожно ущипните кожу в месте инъекции. Другой рукой введите иглу в кожу и надавите на поршень шприца, пока шприц не опустеет.
После инъекции GlucaGen
® : Шаг 11. Вытяните иглу из кожи и надавите на место инъекции.
Вытяните иглу из кожи и надавите на место инъекции.
Выбросьте использованный шприц с присоединенной иглой и любой GlucaGen ® , который вы не использовали. См. « Как следует утилизировать (выбросить) использованные шприцы GlucaGen ® , предварительно заполненные шприцами » в конце этих инструкций.
Шаг 12.Переверните человека на бок. Когда человек без сознания просыпается, его может стошнить. Если повернуть человека на бок, вероятность удушья уменьшится.
Шаг 13. Немедленно вызовите скорую медицинскую помощь.
Шаг 14. Накормите человека, как только он проснется и сможет глотать. Дайте пациенту быстро действующий источник сахара (например, обычный безалкогольный напиток или фруктовый сок) и источник сахара длительного действия (например, крекеры и сыр или мясной бутерброд).
Накормите человека, как только он проснется и сможет глотать. Дайте пациенту быстро действующий источник сахара (например, обычный безалкогольный напиток или фруктовый сок) и источник сахара длительного действия (например, крекеры и сыр или мясной бутерброд).
Шаг 15. Даже если лечение GlucaGen ® разбудит человека, немедленно сообщите об этом врачу. Следует сообщить врачу о сильном падении уровня сахара в крови (реакции гипогликемии).Может потребоваться изменить дозу лекарства от диабета.
Гипогликемия может повториться после приема препарата GlucaGen ® .
Ранние симптомы гипогликемии могут включать:
- потливость
- сонливость
- головокружение
- нарушения сна
- Нерегулярное сердцебиение (сердцебиение)
- тревога
- тремор
- затуманенное зрение
- голод
- невнятная речь
- подавленное настроение
- покалывание в руках, ногах, губах или языке
- раздражительность
- ненормальное поведение
- легкомысленность
- неустойчивое движение
- Невозможность концентрироваться
- изменения личности
- головная боль
- беспокойство
Если не лечить на ранней стадии, гипогликемия может ухудшиться, и у человека может развиться тяжелая гипогликемия. Признаки тяжелой гипогликемии включают:
Признаки тяжелой гипогликемии включают:
Как мне утилизировать (выбросить) предварительно заполненные шприцы GlucaGen
® ?- Поместите использованные шприцы в одобренный FDA контейнер для утилизации острых предметов сразу после использования. Не выбрасывайте (выбрасывайте) незакрепленные иглы и шприцы вместе с домашним мусором.
- Если у вас нет контейнера для утилизации острых предметов, одобренного FDA, вы можете использовать бытовой контейнер:
- из сверхпрочного пластика,
- может закрываться плотно прилегающей, устойчивой к проколам крышкой, при этом острые предметы не выходят наружу,
- вертикально и устойчиво во время использования,
- герметичные и
- должным образом маркирован, чтобы предупредить об опасных отходах внутри контейнера.

- Когда ваш контейнер для утилизации острых предметов будет почти заполнен, вам нужно будет следовать руководящим принципам сообщества, чтобы правильно утилизировать контейнер для утилизации острых предметов. Могут существовать законы штата или местные законы о том, как следует выбрасывать использованные иглы и шприцы. Для получения дополнительной информации о безопасной утилизации острых предметов и конкретной информации об утилизации острых предметов в штате, в котором вы живете, посетите веб-сайт FDA по адресу http: // www.fda.gov/safesharpsdisposal.
- Не выбрасывайте использованный контейнер для утилизации острых предметов в бытовой мусор, если это не разрешено правилами вашего сообщества. Не перерабатывайте использованный контейнер для утилизации острых предметов.
для кошек: отзывы, инструкция по применению
Как известно, кошки обладают от природы совершенно сильным иммунитетом. Но в результате неправильного питания, а также контакта с инфицированными животными здоровый питомец может оказаться в опасности заразиться опасными заболеваниями.Препарат «Гликопин» для кошек, о котором вы можете прочитать в этой статье, считается отличным иммуномодулятором, очень часто назначаемым ветеринарами.
Но в результате неправильного питания, а также контакта с инфицированными животными здоровый питомец может оказаться в опасности заразиться опасными заболеваниями.Препарат «Гликопин» для кошек, о котором вы можете прочитать в этой статье, считается отличным иммуномодулятором, очень часто назначаемым ветеринарами.
Воспользовавшись этим средством для здорового животного, вы максимально повысите его иммунитет, а если ваш любимый кот уже заболел, то это лечебное средство ускорит процесс его выздоровления в несколько раз.
Форма выпуска
Препарат «Гликопин» для кошек, отзывы о котором вы можете прочитать в этой статье, выпускается в виде таблеток в блистерах по десять штук в каждой.Тарелку с таблетками обычно помещают в картонную коробку. Препарат имеет довольно приятный сладкий вкус, поэтому заставлять его принимать животное не придется.
Особенности действия
Когда активные вещества попадают в организм, абсорбируются очень быстро. В течение четырех часов иммунитет животного значительно повышается. Таблетки обладают противовоспалительным, противоинфекционным и противоопухолевым действием. После применения препарата клетки насыщаются кислородом, а также заработают лизосомальные ферменты, уничтожающие огромное количество инородных тел.При этом активируются все иммунные процессы в организме. Большая часть продуктов распада выводится из организма через почки.
Таблетки обладают противовоспалительным, противоинфекционным и противоопухолевым действием. После применения препарата клетки насыщаются кислородом, а также заработают лизосомальные ферменты, уничтожающие огромное количество инородных тел.При этом активируются все иммунные процессы в организме. Большая часть продуктов распада выводится из организма через почки.
В каких случаях назначают препарат
«Гликопин» кошкам, отзывы о которых более положительные, назначают, в первую очередь, для устранения иммунодефицита. Также препарат оправдывает себя сильнейшим отравлением животного, так как повышает сопротивляемость организма опасным инфекциям.
Ветеринары рекомендуют применять препарат «Гликопин» кошкам, по отзывам, описанным в этой статье, в таких случаях:
- при попадании инфекции внутрь;
- при наличии гнойных ран с признаками некроза тканей;
- , если у животного доброкачественные опухоли;
- после хирургической операции;
- для повышения общего иммунитета животного;
- с септическим шоком.

Применяя препарат в качестве профилактики, вы убережете своего питомца от многих болезней.
Несколько слов о назначении
Более подвержены заболеваниям кошки, проживающие на частных территориях. У них повышен иммунитет из-за непогоды, а также из-за холода и дождя. «Гликопин» - таблетки для кошек и собак, которые являются прекрасным средством борьбы с сезонными простудными заболеваниями ваших питомцев.
Препарат придет и на помощь раненым животным. Поврежденные участки начнут быстрее заживать и рубцеваться.В то же время вы заметите, как улучшится шерсть вашего питомца. Он станет гладким и блестящим, исчезнут все грибковые заболевания. Специалисты рекомендуют дать животному перед вязанием средство. Это увеличивает шансы на рождение здоровых котят и щенков.
Инструкция по применению
Чтобы лекарство дало желаемый эффект, а также не причинило вред вашему питомцу, используйте его, точно полагаясь на инструкцию по применению. Если животное не может самостоятельно принимать таблетки, то его придется принудить. Вы можете добавить его в корм своему питомцу или положить ему под язык. Оба метода будут одинаково эффективны.
Вы можете добавить его в корм своему питомцу или положить ему под язык. Оба метода будут одинаково эффективны.
Подбор правильной дозировки
Препарат «Гликопин» (Glikopin), описание которого вы можете прочитать в этой статье, следует применять в правильной дозировке. От этого зависит его эффективность и безопасность.
Дозировка определяется в соответствии с массой животных, а также с основным назначением использования. Маленьким котятам весом до двух килограммов будет достаточно четвертой части таблетки для лечения, а восьмой - для профилактики.Кошкам до трех килограммов подойдет от четверти до половины таблетки. А взрослым кошкам с весом более трех килограммов обычно дают целую таблетку или половину.
Для эффективности лечения животное должно принимать лекарство один раз в день в течение недели. В некоторых случаях срок может быть увеличен или, наоборот, сокращен. Все подробности лечения вам расскажет опытный ветеринар.
Есть ли противопоказания?
Вот описание препарата «Гликопин». Отзывы владельцев домашних животных свидетельствуют о том, что данный препарат нетоксичен, поэтому его безопасно использовать в домашних условиях. Однако следует учитывать, что входящие в его состав вещества могут вызывать аллергические реакции. Также ветеринары не рекомендуют принимать параллельно другие препараты без предварительной консультации, иначе можно нанести животному непоправимый вред.
Отзывы владельцев домашних животных свидетельствуют о том, что данный препарат нетоксичен, поэтому его безопасно использовать в домашних условиях. Однако следует учитывать, что входящие в его состав вещества могут вызывать аллергические реакции. Также ветеринары не рекомендуют принимать параллельно другие препараты без предварительной консультации, иначе можно нанести животному непоправимый вред.
Отзывы
На взрослых кошек «Гликопин» обращают внимание не только хозяева, но и владельцы маленьких котят. Многие пользуются советами ветеринаров и используют эти таблетки как профилактическое средство.После его использования даже кошки, которые много времени проводят на улице, не заражаются инфекционными заболеваниями и простудными заболеваниями.
В Интернете можно найти множество положительных отзывов о препарате, применяемом для лечения пушистых питомцев. Хозяева животных сообщают, что их питомцы очень быстро растут, у них появляется жизненный тонус, улучшается аппетит, нормализуется стул, и болезнь проходит. Однако некоторые владельцы кошек также заметили нежелательные эффекты после применения препарата, которые проявлялись в виде рвоты и диареи.
Однако некоторые владельцы кошек также заметили нежелательные эффекты после применения препарата, которые проявлялись в виде рвоты и диареи.
Таблетки Гликопин: отзывы врачей
Очень часто ветеринары рекомендуют применение препарата «Гликопин» владельцам домашних животных. Средство действительно очень эффективное, проверенное и надежное. Эти таблетки рекомендуется давать котятам, найденным на улице, а также домашним кошкам в профилактических целях. Описано много случаев, когда препарат «Гликопин» спасал жизнь животным. Являясь очень эффективным иммуномодулятором, он значительно повышает защитные силы организма, поэтому процесс выздоровления идет намного быстрее.
Ветеринары советуют владельцам домашних животных пользоваться этим средством после перенесенных операций. Активные компоненты препарата поспособствуют скорейшему выздоровлению вашего питомца. Если вы заботитесь о здоровье котенка или взрослой кошки, не пропустите эти таблетки. С их помощью у вас будет сильное, веселое и счастливое животное. Не запускайте болезнь, лучше проведите профилактические мероприятия. Каждый ветеринар скажет вам, что любое заболевание легче предотвратить, чем лечить.
Не запускайте болезнь, лучше проведите профилактические мероприятия. Каждый ветеринар скажет вам, что любое заболевание легче предотвратить, чем лечить.
Усиление биосинтеза каротиноидов в транспластомных томатах путем индуцированного превращения ликопина в провитамин А
- © 2009 Американское общество биологов растений
Реферат
Каротиноиды - важные пигменты фотосинтетического аппарата и незаменимый компонент питания человека.Помимо того, что они являются мощными антиоксидантами, они также содержат предшественник витамина А β -каротин. В плодах томата ( Solanum lycopersicum ) каротиноиды накапливаются в специализированных пластидах - хромопластах. Как регулируется путь биосинтеза каротиноидов и что ограничивает общее накопление каротиноидов в хромопластах плодов, не совсем понятно. Здесь мы ввели гены ликопина β -циклазы из eubacterium Erwinia herbicola и нарцисса высшего растения ( Narcissus pseudonarcissus ) в геном пластиды томата. Хотя экспрессия бактериального фермента не сильно влияла на состав каротиноидов, экспрессия растительного фермента эффективно превращала ликопин, основной запасной каротиноид плодов томата, в провитамин А ( β, -каротин). В зеленых листьях транспластомных растений томата большее количество ликопина направлялось в β -ветвь биосинтеза каротиноидов, что приводило к увеличению накопления пигментов ксантофиллового цикла и, соответственно, уменьшению накопления ксантофилла лютеина α -ответвления.Во фруктах большая часть ликопина была преобразована в β -каротин с уровнем провитамина А, достигающим 1 мг на грамм сухого веса. Неожиданно транспластомные томаты также показали увеличение общего накопления каротиноидов более чем на 50%, что указывает на то, что экспрессия ликопина β -циклазы усиливает поток через этот путь в хромопластах. Наши результаты дают новое понимание регуляции биосинтеза каротиноидов и демонстрируют потенциал инженерии пластидного генома для улучшения питания пищевых культур.
Хотя экспрессия бактериального фермента не сильно влияла на состав каротиноидов, экспрессия растительного фермента эффективно превращала ликопин, основной запасной каротиноид плодов томата, в провитамин А ( β, -каротин). В зеленых листьях транспластомных растений томата большее количество ликопина направлялось в β -ветвь биосинтеза каротиноидов, что приводило к увеличению накопления пигментов ксантофиллового цикла и, соответственно, уменьшению накопления ксантофилла лютеина α -ответвления.Во фруктах большая часть ликопина была преобразована в β -каротин с уровнем провитамина А, достигающим 1 мг на грамм сухого веса. Неожиданно транспластомные томаты также показали увеличение общего накопления каротиноидов более чем на 50%, что указывает на то, что экспрессия ликопина β -циклазы усиливает поток через этот путь в хромопластах. Наши результаты дают новое понимание регуляции биосинтеза каротиноидов и демонстрируют потенциал инженерии пластидного генома для улучшения питания пищевых культур.
Каротиноиды - это изопреноидные молекулы, которые синтезируются всеми фотосинтезирующими организмами, а также некоторыми грибами и нефотосинтезирующими бактериями. У растений они участвуют в фотосинтетическом сборе света и защите от светового стресса. Кроме того, каротиноиды накапливаются в больших количествах в виде запасных метаболитов в хромопластах цветов, фруктов и стержневых корней. Каротиноиды также необходимы животным, которые, однако, не могут синтезировать их de novo и поэтому должны полагаться на пищевые источники каротиноидов. β -Каротин является основным диетическим предшественником витамина А и поэтому также называется провитамином А. Дефицит витамина А у людей представляет собой глобальную проблему здравоохранения, затрагивающую примерно одну треть стран мира (Mayer et al., 2008 ). Предположительно, благодаря своей антиоксидантной активности, β -каротин и другие виды каротиноидов также обладают защитным действием против сердечно-сосудистых заболеваний, некоторых видов рака и заболеваний, связанных со старением (Collins, 1999).
В то время как энзимология путей биосинтеза каротиноидов у растений и эубактерий в настоящее время достаточно хорошо изучена (Armstrong, 1997; Cunningham and Gantt, 1998; Hirschberg, 2001), понимание регуляции биосинтеза каротиноидов все еще остается довольно низким (Bramley, 2002). ).В основном с использованием плодов томата ( Solanum lycopersicum ) в качестве модельной системы, исследование пигментных мутантов (Ronen et al., 2000; Isaacson et al., 2002; Galpaz et al., 2006) и трансгенных подходов (Giuliano et al. , 2000, 2008; Römer and Fraser, 2005; Fraser et al., 2007) предоставили первое понимание регуляторных механизмов, действующих в каротиногенезе. Например, конститутивная экспрессия гена фитоиндесатуразы ( crtI ) из бактерии Erwinia uredovora приводила к повышенному накоплению β -каротина в томатах, но также приводила к неожиданному снижению общего уровня каротиноидов (Römer et al., 2000). Считается, что снижение общего количества каротиноидов является результатом регуляции с помощью обратной связи от β -каротина или одного из его последующих метаболитов (Bramley, 2002). Однако специфическая для плодов сверхэкспрессия нативной ликопин β -циклазы приводила к увеличению накопления β -каротина без сопутствующего снижения общего количества каротиноидов (Rosati et al., 2000). Почему одни генетические нарушения биосинтеза каротиноидов отрицательно влияют на общее накопление каротиноидов, а другие нет (или даже приводят к увеличению; Dharmapuri et al., 2002; Fraser et al., 2002), еще предстоит установить.
Однако специфическая для плодов сверхэкспрессия нативной ликопин β -циклазы приводила к увеличению накопления β -каротина без сопутствующего снижения общего количества каротиноидов (Rosati et al., 2000). Почему одни генетические нарушения биосинтеза каротиноидов отрицательно влияют на общее накопление каротиноидов, а другие нет (или даже приводят к увеличению; Dharmapuri et al., 2002; Fraser et al., 2002), еще предстоит установить.
Здесь мы использовали трансформацию пластид томата для регулирования биосинтеза каротиноидов на уровне превращения ликопина в β -каротин ферментом ликопином β -циклазы (рис. 1A). Мы показываем, что пластидная экспрессия растительной ликопина β -циклазы не только запускает эффективное преобразование ликопина в β -каротин, но также неожиданно приводит к увеличению общего накопления каротиноидов на> 50%.Это контрастирует с умеренно повышенными уровнями β -каротина и сниженным общим накоплением каротиноидов при экспрессии бактериальной ликопина β -циклазы (Wurbs et al. , 2007) и предполагает, что активность ликопина β -циклазы является важной регуляторной точкой в растении. и микробный биосинтез каротиноидов.
, 2007) и предполагает, что активность ликопина β -циклазы является важной регуляторной точкой в растении. и микробный биосинтез каротиноидов.
Разработка пути биосинтеза каротиноидов путем трансформации пластид. А. Путь биосинтеза каротиноидов у высших растений. Этот путь разделяется на ветвь α и ветвь β непосредственно после ликопина, основного каротиноида-хранилища плодов томата.Фермент, экспрессируемый в пластидном геноме томатов в этом исследовании, ликопин β -циклаза, ведет в ветвь β . B. Физические карты целевой области в пластидном геноме (ptDNA) и векторы трансформации пластид pEcrtY и pNLyc, построенные в этом исследовании. Гены над линией транскрибируются слева направо, гены под линией транскрибируются в противоположном направлении. Трансгены нацелены на межгенную область между генами trnfM и trnfG (Ruf et al., 2001). Ген селектируемого маркера aadA управляется промотором химерного оперона рРНК (P rrn ; Svab and Maliga, 1993), слитым с 3'-UTR гена psbA (T psbA ) и фланкированным двумя сайтами loxP , чтобы сделать возможным удаление маркера с помощью Cre-опосредованной сайт-специфической рекомбинации (Zhou et al. , 2008). Кассета экспрессии трансгена состоит из промотора оперона рибосомной РНК, слитого с 5'-лидером гена 10 фага T7 (P rrn -G10L; Kuroda and Maliga, 2001) и 3'-UTR гена rps16 . (T rps16 ).Указаны сайты рестрикции, используемые для клонирования или анализа RFLP, а гибридизационный зонд, производный от psaB , обозначен горизонтальной чертой. Сайты, утерянные из-за лигирования гетерологичных концов, указаны в скобках. C, Саузерн-блот-анализ транспластомных линий томатов, несущих ген ликопина β -циклазы из нарцисса ( S.l. -pNLyc) или из E. herbicola ( S.l .-pEcrtY). Полную клеточную ДНК расщепляли с помощью Bgl II и гибридизовали с радиоактивно меченным зондом, детектирующим область psaB пластидного генома, которая фланкирует сайт встраивания трансгена (раздел B).Размеры фрагментов указаны в кб. wt, дикий тип. D: Выравнивание (произведенное с помощью ClustalW2) аминокислотных последовательностей ликопин β -циклазы из нарцисса (Np) и E.
, 2008). Кассета экспрессии трансгена состоит из промотора оперона рибосомной РНК, слитого с 5'-лидером гена 10 фага T7 (P rrn -G10L; Kuroda and Maliga, 2001) и 3'-UTR гена rps16 . (T rps16 ).Указаны сайты рестрикции, используемые для клонирования или анализа RFLP, а гибридизационный зонд, производный от psaB , обозначен горизонтальной чертой. Сайты, утерянные из-за лигирования гетерологичных концов, указаны в скобках. C, Саузерн-блот-анализ транспластомных линий томатов, несущих ген ликопина β -циклазы из нарцисса ( S.l. -pNLyc) или из E. herbicola ( S.l .-pEcrtY). Полную клеточную ДНК расщепляли с помощью Bgl II и гибридизовали с радиоактивно меченным зондом, детектирующим область psaB пластидного генома, которая фланкирует сайт встраивания трансгена (раздел B).Размеры фрагментов указаны в кб. wt, дикий тип. D: Выравнивание (произведенное с помощью ClustalW2) аминокислотных последовательностей ликопин β -циклазы из нарцисса (Np) и E. herbicola (Eh). Звездочка (*) обозначает остатки, идентичные в обеих последовательностях (выделены жирным шрифтом), двоеточие (:) указывает на консервативные замены, а точка указывает на полуконсервативные замены. N-концевое удлинение последовательности Np, вероятно, содержит транзитный пептид для импорта белка в пластиды. Аминокислоты, которые изменились из-за коррекции последовательности Lyc из нарцисса (опубликованная последовательность: номер доступа GenBank.X98796.1; исправленная последовательность: инвентарный номер GQ327929) подчеркнуты. Исправления улучшают сходство последовательностей в N-концевых доменах последовательностей Np и Eh.
herbicola (Eh). Звездочка (*) обозначает остатки, идентичные в обеих последовательностях (выделены жирным шрифтом), двоеточие (:) указывает на консервативные замены, а точка указывает на полуконсервативные замены. N-концевое удлинение последовательности Np, вероятно, содержит транзитный пептид для импорта белка в пластиды. Аминокислоты, которые изменились из-за коррекции последовательности Lyc из нарцисса (опубликованная последовательность: номер доступа GenBank.X98796.1; исправленная последовательность: инвентарный номер GQ327929) подчеркнуты. Исправления улучшают сходство последовательностей в N-концевых доменах последовательностей Np и Eh.
РЕЗУЛЬТАТЫ
Введение генов ликопина
β -циклазы в пластидный геном томата Недавний транскриптомический и трансатомический анализ экспрессии пластидных генов во время созревания плодов томатов показал, что большинство генов в пластидном геноме резко подавляются во время развития плодов (Kahlau and Bock, 2008). Однако это исследование также идентифицировало небольшое количество пластидных элементов экспрессии (промоторов и сигналов инициации трансляции), которые остаются активными в хромопластах (Kahlau and Bock, 2008). Поскольку предыдущая попытка экспрессии гена ликопина β -циклазы ( crtY ) из продуцирующей каротиноиды эубактерии Erwinia herbicola привела только к умеренному увеличению накопления β -каротина (до 280 нг / мг сухого вещества). weight), мы хотели проверить, можно ли улучшить уровни экспрессии трансгена с помощью промотора, который сохраняет более высокую активность в хромопластах, чем ранее использованный промотор atpI (Wurbs et al., 2007). Поскольку рибосомные РНК представляют собой наиболее распространенные виды пластидных РНК в хромопластах (Kahlau and Bock, 2008), мы выбрали промотор оперона рРНК и объединили его с самым сильным известным сайтом связывания с рибосомами, последовательностью Шайна-Далгарно из гена 10 бактериофага T7.
Однако это исследование также идентифицировало небольшое количество пластидных элементов экспрессии (промоторов и сигналов инициации трансляции), которые остаются активными в хромопластах (Kahlau and Bock, 2008). Поскольку предыдущая попытка экспрессии гена ликопина β -циклазы ( crtY ) из продуцирующей каротиноиды эубактерии Erwinia herbicola привела только к умеренному увеличению накопления β -каротина (до 280 нг / мг сухого вещества). weight), мы хотели проверить, можно ли улучшить уровни экспрессии трансгена с помощью промотора, который сохраняет более высокую активность в хромопластах, чем ранее использованный промотор atpI (Wurbs et al., 2007). Поскольку рибосомные РНК представляют собой наиболее распространенные виды пластидных РНК в хромопластах (Kahlau and Bock, 2008), мы выбрали промотор оперона рРНК и объединили его с самым сильным известным сайтом связывания с рибосомами, последовательностью Шайна-Далгарно из гена 10 бактериофага T7. (Курода, Малига, 2001; Oey et al., 2009; рис. 1Б). Помимо гена ликопина β -циклазы из E. herbicola , мы также клонировали ген Lyc ликопина β -циклазы из нарцисса высших растений ( Narcissus pseudonarcissus ; Al-Babili et al., 1996; любезно предоставлено доктором. Peter Beyer и Salim Al-Babili, University of Freiburg, Germany) в одну и ту же кассету экспрессии (рис. 1B). Когда мы повторно секвенировали оба гена после завершения конструирования вектора, мы отметили три однонуклеотидных отклонения от опубликованной последовательности Lyc (номер доступа GenBank X98796.1). Все три отклонения также присутствовали в исходном клоне Lyc и предположительно представляют собой ошибки из-за сжатия полос в гелях для секвенирования: C отсутствовал после положения 442 (три C вместо двух C в опубликованной последовательности), G отсутствовал после положения 447 (три G вместо двух G в опубликованной последовательности), а C отсутствовал после положения 480 (два C вместо одного C в опубликованной последовательности).
(Курода, Малига, 2001; Oey et al., 2009; рис. 1Б). Помимо гена ликопина β -циклазы из E. herbicola , мы также клонировали ген Lyc ликопина β -циклазы из нарцисса высших растений ( Narcissus pseudonarcissus ; Al-Babili et al., 1996; любезно предоставлено доктором. Peter Beyer и Salim Al-Babili, University of Freiburg, Germany) в одну и ту же кассету экспрессии (рис. 1B). Когда мы повторно секвенировали оба гена после завершения конструирования вектора, мы отметили три однонуклеотидных отклонения от опубликованной последовательности Lyc (номер доступа GenBank X98796.1). Все три отклонения также присутствовали в исходном клоне Lyc и предположительно представляют собой ошибки из-за сжатия полос в гелях для секвенирования: C отсутствовал после положения 442 (три C вместо двух C в опубликованной последовательности), G отсутствовал после положения 447 (три G вместо двух G в опубликованной последовательности), а C отсутствовал после положения 480 (два C вместо одного C в опубликованной последовательности). Эти вставки изменяют опубликованную последовательность белка на отрезке из 12 аминокислот (рис. 1D; так как всего три нуклеотида отсутствуют, опубликованная последовательность возвращается в правильную рамку считывания в положении нуклеотида 481). Исправленная последовательность Lyc была депонирована в базе данных GenBank (номер доступа GQ327929).
Эти вставки изменяют опубликованную последовательность белка на отрезке из 12 аминокислот (рис. 1D; так как всего три нуклеотида отсутствуют, опубликованная последовательность возвращается в правильную рамку считывания в положении нуклеотида 481). Исправленная последовательность Lyc была депонирована в базе данных GenBank (номер доступа GQ327929).
Кассеты экспрессии пластид, содержащие трансгены crtY и Lyc , вставляли в плазмиду pKP9 (Zhou et al., 2008), генерируя векторы трансформации хлоропластов pEcrtY и pNLyc, соответственно (Fig. 1B). Две конструкции были введены в пластидный геном коммерческого томата сорта IPA-6 путем биолистической трансформации хлоропластов (Svab, Maliga, 1993; Ruf et al., 2001). Одиннадцать транспластомных линий были получены с помощью pEcrtY (из 400 селекционных планшетов с бомбардированными частями листьев) и 22 транспластомных линии были получены с помощью pNLyc (из 350 селекционных планшетов). Подробно охарактеризованы три независимо генерируемые линии на конструкцию. В дальнейшем линии будут называться S.l. -pNLyc (для Solanum lycopersicum , несущего ген Narcissus Lyc ) и S.l. -pEcrtY (для Solanum lycopersicum , несущего ген Erwinia crtY ).
В дальнейшем линии будут называться S.l. -pNLyc (для Solanum lycopersicum , несущего ген Narcissus Lyc ) и S.l. -pEcrtY (для Solanum lycopersicum , несущего ген Erwinia crtY ).
Анализ транспластомных растений томатов, содержащих ликопин
β -циклаза трансгены Предполагаемые трансформанты хлоропластов очищали до гомоплазии, пропуская их через дополнительные циклы регенерации при выборе антибиотика.Трансформация генома хлоропласта, правильная интеграция трансгенов посредством гомологичной рекомбинации и гомоплазмия транспластомных линий (то есть отсутствие остаточных копий генома хлоропласта дикого типа) были оценены с помощью анализа RFLP (рис. 1C), и гомоплазмия была дополнительно подтверждена. анализом семян (рис. 2А). Отсутствие сегрегации устойчивости к антибиотикам в поколении T1 продемонстрировало гомоплазмию (рис. 2A) и подтвердило наследование материнского трансгена, как и ожидалось для признака, кодируемого пластидами у томатов. Гомоплазматические растения Т1 из С.л. -pNLyc и S.l. Транспластомные линии -pEcrtY были неотличимы от контроля дикого типа (фиг. 2В), что указывает на то, что экспрессия трансгена фенотипически нейтральна.
Гомоплазматические растения Т1 из С.л. -pNLyc и S.l. Транспластомные линии -pEcrtY были неотличимы от контроля дикого типа (фиг. 2В), что указывает на то, что экспрессия трансгена фенотипически нейтральна.
Гомоплазма и фенотипы транспластомных линий томатов. А. Примеры тестов семян для подтверждения гомоплазмы. Семена дикого типа ( S.l., мас.) И транспластомных растений, полученных с использованием конструкций pEcrtY и pNLyc, проращивали на среде со спектиномицином (100 мг / л).Устойчивость к антибиотикам и отсутствие сегрегации в поколении T1 подтверждает гомоплазматическое состояние транспластомных линий. В. Фенотип дикого типа гомоплазматических линий томатов, экспрессирующих трансгены ликопина β -циклазы из их пластидных геномов.
Для анализа экспрессии введенных генов биосинтеза каротиноидов мы сначала провели серию экспериментов с гель-блоттингом РНК. Анализ экспрессии трансгена в листьях выявил накопление стабильной моноцистронной мРНК и присутствие дополнительных видов с более длинными транскриптами, происходящих из сквозной транскрипции, что также наблюдалось в предыдущих экспериментах по трансформации пластид с векторами, которые нацелены на тот же сайт встраивания в геноме (Wurbs и другие. , 2007; Чжоу и др., 2008; Рис. 3A). Те же два основных вида РНК также обнаруживаются в спелых фруктах, хотя наличие более выраженного мазка в области с низким уровнем M r может указывать на более высокий оборот транскриптов в хромопластах (рис. 3B).
, 2007; Чжоу и др., 2008; Рис. 3A). Те же два основных вида РНК также обнаруживаются в спелых фруктах, хотя наличие более выраженного мазка в области с низким уровнем M r может указывать на более высокий оборот транскриптов в хромопластах (рис. 3B).
Анализ накопления мРНК ликопина β -циклазы в листьях (A) и спелых плодах (B) транспластомных растений томата. Полную клеточную РНК гибридизовали с радиоактивно меченными зондами, соответствующими кодирующим областям crtY или Lyc .С помощью каждого зонда выявляются два основных вида транскриптов. В то время как нижняя полоса представляет мРНК зрелой моноцистронной ликопина β -циклазы (1,3 т.п.н. для crtY и 1,7 т.п.н. для Lyc ), верхняя полоса, скорее всего, представляет собой стабильный транскрипт считывания, как это наблюдалось ранее с pKP9. -производные векторы (Zhou et al., 2008; Oey et al., 2009). Размеры полос маркеров указаны в тб. Обратите внимание, что crtY и Lyc не перекрестно гибридизуются из-за недостаточного сходства последовательностей (рис.1D). wt, дикий тип.
Обратите внимание, что crtY и Lyc не перекрестно гибридизуются из-за недостаточного сходства последовательностей (рис.1D). wt, дикий тип.
Затем мы хотели проверить повышенную активность ликопина β -циклазы в транспластомных растениях томатов. С этой целью мы обрабатывали проростки гербицидом 2- (4-хлорфенилтио) триэтиламином (CPTA), специфическим ингибитором ликопенциклазы (Schuetz, Baldwin, 1958; Wurbs et al., 2007). В то время как S.l. Транспластомные растения -pEcrtY показали только умеренно повышенную устойчивость к CPTA по сравнению с диким типом, S.l. Растения -pNLyc проявляли огромную устойчивость к гербициду.В то время как отбеливатели дикого типа уже при концентрации CPTA 50 мкМ м, мкл. На растения -pNLyc практически не влияли концентрации до 500 мкл м CPTA (рис. 4). Это предварительно предполагает, что активность ликопина β -циклазы резко повышена в S.l. -pNLyc транспластомных растений, но не сильно увеличился в S. l. -pEcrtY растения.
l. -pEcrtY растения.
Анализы устойчивости к гербицидам для проверки экспрессии ликопина β -циклазы.Гербицид СРТА использовали в качестве специфического ингибитора активности ликопин β -циклазы. Растения томатов, выращенные в асептических условиях, поливали 2,5 мл раствора СРТА для получения указанных конечных концентраций (50, 100, 150, 250 или 500 мкм мкм). Фенотипическое сравнение с обработанным водой контролем (0 мкм мкм) проводили через 7 дней. wt, дикий тип.
Биосинтез каротиноидов в плодах транспластомных растений томата
Темно-красный каротиноид ликопин представляет собой основной запасающий каротиноид в плодах томатов.Наличие повышенных уровней активности ликопина β -циклазы в плодах должно приводить к усиленному превращению ликопина в апельсиновый каротиноид β -каротин (провитамин A; рис. 1A). Изучение спелых плодов наших транспластомных растений томатов показало, что S. l. Томаты -pNLyc были ярко-оранжевыми вместо темно-красных (рис. 5). Напротив, S.l. Транспластомные томаты -pEcrtY практически не отличались от томатов дикого типа (рис.5). Взятые вместе с результатами анализов CPTA, это позволяет предположить, что нарциссциклаза экспрессировалась на высоких уровнях и была высокоактивна в пластидах томатов.
l. Томаты -pNLyc были ярко-оранжевыми вместо темно-красных (рис. 5). Напротив, S.l. Транспластомные томаты -pEcrtY практически не отличались от томатов дикого типа (рис.5). Взятые вместе с результатами анализов CPTA, это позволяет предположить, что нарциссциклаза экспрессировалась на высоких уровнях и была высокоактивна в пластидах томатов.
Фенотипы плодов томата из транспластомных растений томата, экспрессирующие трансгены ликопина β -циклазы. Плоды дикого растения ( S.l., мас.), S.l. -pEcrtY и S.l. Линию -pNLyc собирали на разных стадиях созревания и фотографировали сбоку (верхний ряд) и снизу (нижний ряд).Оранжевый цвет спелых S.l. -pNLyc плодов указывает на эффективное преобразование красного ликопина в оранжевый β -каротин (провитамин А).
Чтобы определить, в какой степени пластидная экспрессия трансгенов ликопина β -циклазы привела к изменению содержания или состава каротиноидов в томатах, мы измерили накопление каротиноидов в плодах с помощью ВЭЖХ. В то время как каротиноидный состав в с.л. -pEcrtY томатов существенно не отличался от такового в томатах дикого типа, экспрессия нарциссы циклазы приводила к резкому увеличению накопления β -каротина (достигая 1 мг на г сухой массы) и сопутствующему снижению накопления ликопина ( Инжир.6А). Однако неожиданно эти изменения не были пропорциональны тому, что увеличение β -каротина значительно превышало уменьшение ликопина. Следовательно, S.l. Томаты -pNLyc имели гораздо более высокое общее содержание каротиноидов (увеличение на 52% по сравнению с диким типом; фиг. 6A). Это предполагает, что пластидная экспрессия циклазы нарциссов не только запускает эффективное превращение ликопина в - β -каротин, но также приводит к общему усилению пути биосинтеза каротиноидов в плодах.
В то время как каротиноидный состав в с.л. -pEcrtY томатов существенно не отличался от такового в томатах дикого типа, экспрессия нарциссы циклазы приводила к резкому увеличению накопления β -каротина (достигая 1 мг на г сухой массы) и сопутствующему снижению накопления ликопина ( Инжир.6А). Однако неожиданно эти изменения не были пропорциональны тому, что увеличение β -каротина значительно превышало уменьшение ликопина. Следовательно, S.l. Томаты -pNLyc имели гораздо более высокое общее содержание каротиноидов (увеличение на 52% по сравнению с диким типом; фиг. 6A). Это предполагает, что пластидная экспрессия циклазы нарциссов не только запускает эффективное превращение ликопина в - β -каротин, но также приводит к общему усилению пути биосинтеза каротиноидов в плодах.
Анализ ВЭЖХ накопления пигмента в плодах и листьях растений дикого типа ( S.l. -wt) и транспластомных S.l. -pEcrtY и S.l. -pNLyc растения. А. Сравнение содержания ликопина и β -каротина (в нг / мг сухого веса [DW]) в спелых фруктах, как определено с помощью ВЭЖХ. Значения представляют собой средние значения из 12 измерений: три плода, собранные от трех до четырех независимых линий растений на конструкцию. B, Сравнение содержания каротиноидов в листьях.Значения представляют собой средние значения из девяти измерений, которые включают листья, собранные по меньшей мере из четырех независимых транспластомных линий на конструкцию. SD отображается как полоса ошибок. Звездочки указывают на значительные различия по сравнению с диким типом (значение P <0,05).
А. Сравнение содержания ликопина и β -каротина (в нг / мг сухого веса [DW]) в спелых фруктах, как определено с помощью ВЭЖХ. Значения представляют собой средние значения из 12 измерений: три плода, собранные от трех до четырех независимых линий растений на конструкцию. B, Сравнение содержания каротиноидов в листьях.Значения представляют собой средние значения из девяти измерений, которые включают листья, собранные по меньшей мере из четырех независимых транспластомных линий на конструкцию. SD отображается как полоса ошибок. Звездочки указывают на значительные различия по сравнению с диким типом (значение P <0,05).
Биосинтез каротиноидов в листьях транспластомных растений томата
Затем мы хотели определить, влияет ли избыточная экспрессия ликопина β -циклазы на биосинтез каротиноидов также в листьях.При анализе ткани листа транспластомных растений, экспрессирующих ген циклазы Erwinia , было обнаружено, что состав каротиноидов не изменился (фиг. 6B). Напротив, уходит из S.l. У растений -pNLyc наблюдались выраженные изменения пигментного состава. Хотя содержание хлорофилла было идентично дикому типу (данные не показаны), спектры каротиноидов показали значительно повышенные уровни виолаксантина, антераксантина и зеаксантина каротиноидов цикла ксантофилла, а также значительное снижение накопления лютеина (рис.6Б). Эти изменения пропорциональны тем, что не влекут за собой значительного изменения общего содержания каротиноидов в листьях. Это говорит о том, что в S.l. -pNLyc, поток через β -ветвь пути биосинтеза каротиноидов (рис. 1A) увеличивается, а поток через α -ветвь пропорционально уменьшается.
6B). Напротив, уходит из S.l. У растений -pNLyc наблюдались выраженные изменения пигментного состава. Хотя содержание хлорофилла было идентично дикому типу (данные не показаны), спектры каротиноидов показали значительно повышенные уровни виолаксантина, антераксантина и зеаксантина каротиноидов цикла ксантофилла, а также значительное снижение накопления лютеина (рис.6Б). Эти изменения пропорциональны тем, что не влекут за собой значительного изменения общего содержания каротиноидов в листьях. Это говорит о том, что в S.l. -pNLyc, поток через β -ветвь пути биосинтеза каротиноидов (рис. 1A) увеличивается, а поток через α -ветвь пропорционально уменьшается.
ОБСУЖДЕНИЕ
В данной работе мы экспрессировали два гена ликопина β -циклазы из пластидного генома томата.В то время как ген из эубактерии Erwinia не привел к значительному изменению накопления каротиноидов, экспрессия ликопина β -циклазы из нарцисса высших растений не только запускала эффективное превращение ликопина в провитамин А, но и приводила к значительному увеличению общего содержания каротиноидов в плодах.
Отсутствие эффективной экспрессии гена Erwinia было неожиданным, потому что более ранняя попытка превратить ликопин в β -каротин путем экспрессии этого гена из пластидного генома привела по крайней мере к умеренному увеличению β - накопление каротина (до 286 мк г / г сухой массы), хотя общий уровень каротиноидов снизился более чем на 10% (Wurbs et al., 2007). Ликопин β -циклазы из Erwinia и Narcissus обладают значительным сходством последовательностей на уровне белка (рис. 1D), но сходство на уровне ДНК очень низкое. Низкая устойчивость к CPTA модели S.l. Растения -pEcrtY (рис. 4) явно указывают на проблему с накоплением белка. Используемые здесь промотор и 5'-нетранслируемая область (UTR) должны были вызывать более сильную экспрессию, чем использованный ранее промотор atpI (Kahlau and Bock, 2008; Oey et al., 2009), и не совсем понятно, почему этого не произошло. Одна из возможных причин может заключаться в том, что доступность последовательности Шайна-Дальгарно для пластидных рибосом нарушена в контексте последовательности P rrn -G10L, например, из-за образования аберрантной вторичной структуры между 5'-UTR и кодированием crtY область, край. Было продемонстрировано, что маскирование последовательности Шайна-Далгарно за счет образования вторичной структуры РНК эффективно предотвращает трансляцию у обеих бактерий (Hall et al., 1982) и пластиды (Hirose, Sugiura, 1997). Поскольку аберрантное сворачивание РНК, как известно, трудно предсказать и практически невозможно проанализировать in vivo, его возможное участие в отсутствии экспрессии crtY из кассеты P rrn -G10L в дальнейшем не исследовалось.
Было продемонстрировано, что маскирование последовательности Шайна-Далгарно за счет образования вторичной структуры РНК эффективно предотвращает трансляцию у обеих бактерий (Hall et al., 1982) и пластиды (Hirose, Sugiura, 1997). Поскольку аберрантное сворачивание РНК, как известно, трудно предсказать и практически невозможно проанализировать in vivo, его возможное участие в отсутствии экспрессии crtY из кассеты P rrn -G10L в дальнейшем не исследовалось.
Интересно, что пластидная экспрессия ликопина β -циклазы нарциссов привела к сильному увеличению общего содержания каротиноидов в плодах. Это было неожиданно, поскольку предыдущая экспрессия ликопин β -циклазы из Erwinia приводила к более низкому общему содержанию каротиноидов (Wurbs et al., 2007). Правдоподобное объяснение может заключаться в том, что фермент нарциссов менее восприимчив к регуляции отрицательной обратной связи β -каротином, чем бактериальный фермент. Это также может быть совместимо с высоким накоплением β -каротина (и общего каротиноида), которое фермент нарциссов запускает в хромопластах цветков. Ликопин β -циклаза нарциссов, таким образом, может предоставить ценный инструмент для улучшения метаболического пути каротиноидов во фруктах.
Это также может быть совместимо с высоким накоплением β -каротина (и общего каротиноида), которое фермент нарциссов запускает в хромопластах цветков. Ликопин β -циклаза нарциссов, таким образом, может предоставить ценный инструмент для улучшения метаболического пути каротиноидов во фруктах.
Экспрессия ликопина β -циклазы нарциссов также приводила к изменению состава каротиноидов в листьях.Накопление пигментов ксантофиллового цикла зеаксантина, антераксантина и виолаксантина было увеличено, а накопление α -ветвевого ксантофилла лютеина было соответственно снижено (рис. 1А). В листьях превращение ликопина в β -каротин и α -каротин обычно является полным, поскольку ликопин не обнаруживается. Очевидно, существует субстратная конкуренция между ликопином β -циклазой и ликопен ϵ -циклазой, и поэтому присутствие повышенных количеств ликопина β -циклазы достаточно для направления большего количества ликопина в β -ответвление каротиноида. биосинтез.Это изменение прохождения по пути не привело к какому-либо фенотипическому эффекту, что не является неожиданным, поскольку лютеин, вид пигмента, уменьшился в S.l. Ранее было показано, что растения -pNLyc незаменимы для фотосинтеза у высших растений (Pogson et al., 1996).
биосинтез.Это изменение прохождения по пути не привело к какому-либо фенотипическому эффекту, что не является неожиданным, поскольку лютеин, вид пигмента, уменьшился в S.l. Ранее было показано, что растения -pNLyc незаменимы для фотосинтеза у высших растений (Pogson et al., 1996).
Как повышение содержания провитамина А, так и увеличение общего содержания каротиноидов в томатах представляют собой важные цели селекционной и генной инженерии (Ye et al., 2000; Giuliano et al., 2008; Mayer et al., 2008). Получение с помощью инженерии пластидного генома коммерческого сорта томатов уровней провитамина А, приближающихся к 1 мг / г сухого веса, и, в то же время, увеличение общего содержания каротиноидов в плодах более чем на 50%, следовательно, также является обнадеживающим шагом вперед в метаболическая инженерия каротиноидного пути в томате. Учитывая, что примерно 10 мг β -каротина в день обеспечивает рекомендованную для взрослых диетическую норму витамина А (http://www. nlm.nih.gov/medlineplus/druginfo/natural/patient-vitamina.html), S.l. Томаты -pNLyc являются очень богатым источником провитамина А. Экспрессия ликопина нарциссов β -циклаза представляет собой лишь второй (и на сегодняшний день наиболее успешный) пример метаболической инженерии путем трансформации пластид в пищевых культурах (Wurbs et al. ., 2007). Это связано с тем, что табак ( Nicotiana tabacum ) по-прежнему является единственным растением, в котором трансформация пластид является рутинной. Создание транспластомных растений у немногих других видов, которые могут быть трансформированы, намного сложнее, трудоемко и требует много времени (Ruf et al., 2001; Dufourmantel et al., 2005). Однако, поскольку транспластомная технология предлагает уникальные преимущества, включая накопление высокого уровня чужеродного белка (до> 70% от общего растворимого белка в растении; Oey et al., 2009), отсутствие эпигенетических эффектов, удобное наложение трансгенов в опероны, и значительно увеличенное содержание трансгенов из-за материнской наследования пластидных генов (Ruf et al.
nlm.nih.gov/medlineplus/druginfo/natural/patient-vitamina.html), S.l. Томаты -pNLyc являются очень богатым источником провитамина А. Экспрессия ликопина нарциссов β -циклаза представляет собой лишь второй (и на сегодняшний день наиболее успешный) пример метаболической инженерии путем трансформации пластид в пищевых культурах (Wurbs et al. ., 2007). Это связано с тем, что табак ( Nicotiana tabacum ) по-прежнему является единственным растением, в котором трансформация пластид является рутинной. Создание транспластомных растений у немногих других видов, которые могут быть трансформированы, намного сложнее, трудоемко и требует много времени (Ruf et al., 2001; Dufourmantel et al., 2005). Однако, поскольку транспластомная технология предлагает уникальные преимущества, включая накопление высокого уровня чужеродного белка (до> 70% от общего растворимого белка в растении; Oey et al., 2009), отсутствие эпигенетических эффектов, удобное наложение трансгенов в опероны, и значительно увеличенное содержание трансгенов из-за материнской наследования пластидных генов (Ruf et al. , 2007), очевидно, есть убедительные доводы в пользу дальнейшего развития технологии трансформации пластид и ее применения в сельском хозяйстве и биотехнологии.Наши данные, представленные здесь, демонстрируют, что при выборе подходящих комбинаций трансгенов и элементов экспрессии эффективная метаболическая инженерия посредством трансформации пластид также возможна в незеленых тканях.
, 2007), очевидно, есть убедительные доводы в пользу дальнейшего развития технологии трансформации пластид и ее применения в сельском хозяйстве и биотехнологии.Наши данные, представленные здесь, демонстрируют, что при выборе подходящих комбинаций трансгенов и элементов экспрессии эффективная метаболическая инженерия посредством трансформации пластид также возможна в незеленых тканях.
МАТЕРИАЛЫ И МЕТОДЫ
Растительный материал
Растения томатов, выращенных в асептических условиях ( Solanum lycopersicum ‘IPA-6’), получали из стерилизованных на поверхности семян, проращенных и выращенных на отвержденной агаром среде Murashige и Skoog (Murashige and Skoog, 1962) с 20 г / л Suc.Гомоплазматические транспластомные линии укореняли и размножали на тех же средах. Укоренившиеся гомоплазматические растения переносили в почву и выращивали до зрелости в стандартных тепличных условиях (250 мкм моль квантов м -2 с -1 ). Плоды собирали на разных стадиях созревания.
Плоды собирали на разных стадиях созревания.
Процедуры клонирования
Кодирующая область гена crtY из Erwinia herbicola была вырезана как фрагмент Nco I / Xba I из ранее описанной плазмиды (Wurbs et al., 2007), клонировали в кассету экспрессии, управляемую P rrn -G10L (Kuroda and Maliga, 2001; Oey et al., 2009), а затем интегрировали как фрагмент Sac I / Hin dIII в ранее описанный вектор трансформации пластид pKP9 (Zhou et al., 2008), генерирующий вектор pEcrtY (рис. 1C). Клонированный ген ликопина β -циклазы ( Lyc ) из нарциссов ( Narcissus pseudonarcissus ; любезно предоставлен докторами Питером Бейером и Салимом Аль-Бабили, Университет Фрайбурга, Германия) амплифицировали с помощью ПЦР с праймерами PNlyc5 ′ ( 5'-TTTTCCATGGATACTCTATTGAGAACCCA-3 ') и PNlyc3' (5'-TTTTACTAGTCCCTATCTTGAACTAAGTTA-3 ').С последовательностями праймеров были введены сайт рестрикции 5 ' Nco I и сайт 3' Spe I (подчеркнуты). Вся кодирующая область гена Lyc (включая предполагаемую последовательность транзитного пептида) была клонирована в ту же кассету экспрессии P rrn -G10L (как фрагмент Nco I / Spe I в Nco I / Xba I-переваренный вектор) и затем интегрировали в pKP9 в виде фрагмента Sac I / Apa I, генерируя вектор трансформации pNLyc (рис.1С).
Вся кодирующая область гена Lyc (включая предполагаемую последовательность транзитного пептида) была клонирована в ту же кассету экспрессии P rrn -G10L (как фрагмент Nco I / Spe I в Nco I / Xba I-переваренный вектор) и затем интегрировали в pKP9 в виде фрагмента Sac I / Apa I, генерируя вектор трансформации pNLyc (рис.1С).
Трансформация хлоропластов томатов
Пластидную трансформацию проводили с использованием биолистического протокола (Сваб и Малига, 1993; Руф и др., 2001). Молодые листья томатов, выращенных в асептических условиях, бомбардировали покрытыми плазмидной ДНК частицами золота размером 0,6- мкм мкм, используя биолистический пистолет с адаптером Hepta (PDS1000He; Bio-Rad). Линии томатов, устойчивые к спектиномицину, отбирали на модифицированной среде Мурашиге и Скуга (Wurbs et al., 2007), содержащий спектиномицин (500 мг / л). Для каждой конструкции несколько независимых транспластомных линий томатов подвергали трем дополнительным циклам регенерации на среде, содержащей спектиномицин, для получения гомоплазматической ткани. Гомоплазмия была подтверждена анализами наследования (Bock, 2001), в которых семена проращивали на среде Мурасиге и Скуга, содержащей спектиномицин (100 мг / л).
Гомоплазмия была подтверждена анализами наследования (Bock, 2001), в которых семена проращивали на среде Мурасиге и Скуга, содержащей спектиномицин (100 мг / л).
Выделение нуклеиновых кислот и гель-блот анализ
Тотальную ДНК растений выделяли из образцов свежей ткани листа с помощью метода на основе цетилтриметиламмонийбромида (Doyle and Doyle, 1990).Полную клеточную РНК экстрагировали с использованием реагента peqGOLD TriFast (Peqlab GmbH). Для саузерн-блот-анализа образцы общей ДНК 5 мкл г расщепляли рестрикционным ферментом Bgl II, разделяли гель-электрофорезом на 1% агарозном геле и переносили на нейлоновые мембраны Hybond (GE Healthcare) капиллярным блоттингом. Образцы полной клеточной РНК подвергали электрофорезу в 1% агарозных гелях, содержащих формальдегид, и наносили на нейлоновые мембраны Hybond. Гибридизацию проводили при 65 ° C в буфере Черча (Church and Gilbert, 1984).Зонды для гибридизации очищали электрофорезом в агарозном геле после экстракции представляющих интерес фрагментов ДНК из вырезанных срезов геля с использованием набора GFX PCR (очистка ДНК и полос геля) (GE Healthcare). Продукт ПЦР длиной 550 п.н., полученный амплификацией части кодирующей области psaB с использованием праймеров P7247 и P7244 (Wurbs et al., 2007), использовали в качестве зонда RFLP для проверки трансформации пластид и оценки гомоплазмы. Трансген-специфические зонды для анализа методом Нозерн-блоттинга были получены путем вырезания кодирующих областей Erwinia и Narcissus -циклазы β -циклазы из плазмидных клонов с помощью Nco I и Xba I.
Продукт ПЦР длиной 550 п.н., полученный амплификацией части кодирующей области psaB с использованием праймеров P7247 и P7244 (Wurbs et al., 2007), использовали в качестве зонда RFLP для проверки трансформации пластид и оценки гомоплазмы. Трансген-специфические зонды для анализа методом Нозерн-блоттинга были получены путем вырезания кодирующих областей Erwinia и Narcissus -циклазы β -циклазы из плазмидных клонов с помощью Nco I и Xba I.
Анализ толерантности к гербицидам
Синтез химического соединения CPTA, как специфического ингибитора ликопенциклазы, был описан ранее (Schuetz and Baldwin, 1958; Wurbs et al., 2007). Толерантность транспластомных растений томатов к СРТА оценивали путем добавления 2,5 мл раствора СРТА к растениям, выращенным в асептических условиях в ящиках на среде 2 × Murashige и Skoog (для получения конечных концентраций гербицидов 50, 100, 150, 250 или 500 мкл m) с последующим фенотипическим сравнением с контролем, обработанным водой, через 7 дней.
Анализ пигментов ВЭЖХ
Каротиноиды и хлорофиллы были выделены из ткани листа (замороженной, измельченной и лиофилизированной) экстракцией 80% ацетоном с последующими двумя дополнительными экстракциями 100% ацетоном и комбинацией трех экстрактов. Ткань плодов томатов, собранных в начале размягчения плодов, замораживали, измельчали, лиофилизировали и экстрагировали, как описано выше. Разделение, идентификация и количественное определение каротиноидов выполняли с помощью ВЭЖХ с использованием системы ВЭЖХ Agilent серии 1100 с блоком обнаружения диодной матрицы (Agilent).Для всех разделений использовали колонку YMC ODS-A 250 × 4,6 мм + предколонку. Разделение проводили, как описано ранее (Wurbs et al., 2007). Все виды пигментов были идентифицированы и количественно определены путем сравнения с известными количествами чистых стандартов.
Данные последовательности из этой статьи можно найти в библиотеках данных GenBank / EMBL под номером доступа GQ327929.
Благодарности
Мы благодарны докторам. Питер Бейер и Салим Аль-Бабили (Университет Фрайбурга, Германия) за предоставление клона ликопинциклазы нарциссов.Мы благодарим доктора Стефани Руф и Штеффи Сигер (Max-Planck-Institut für Molekulare Pflanzenphysiologie) за помощь в трансформации растений, Helga Kulka (Max-Planck-Institut für Molekulare Pflanzenphysiologie Green Team) за уход и выращивание растений, Йозефа Бергштейна (Max- Planck-Institut für Molekulare Pflanzenphysiologie) за фотографию и Йоси Хиршберга (Еврейский университет Иерусалима) за полезные обсуждения и критическое прочтение рукописи.
Сноски
Автор, ответственный за распространение материалов, относящихся к результатам, представленным в этой статье, в соответствии с политикой, описанной в Инструкциях для авторов (www.plantphysiol.org): Ральф Бок (rbock {at} mpimp-golm.mpg.de).
www.plantphysiol.org/cgi/doi/10.
 1104/pp.109.140533
1104/pp.109.140533№1 Работа поддержана Обществом Макса Планка и Deutsche Forschungsgemeinschaft (грант № BO 1482 / 11–1, предоставленный R.B.).
↵ [OA] Статьи в открытом доступе можно просматривать в Интернете без подписки.
- Поступила 28.04.2009.
- Принята 6 июля 2009 г.
- Опубликована 8 июля 2009 г.
ЦИФРОВАЯ ЛИТЕРАТУРА
- ↵
Аль-Бабили С., Хобейка Е., Бейер П. (1996) кДНК, кодирующая ликопинциклазу из Narcissus pseudonarcissus L. (PGR96-107). Физиология растений 112 : 1398
- ↵
Armstrong GA (1997) Генетика биосинтеза эубактериальных каротиноидов: красочная история.
 Annu Rev Microbiol 51 : 629–659
Annu Rev Microbiol 51 : 629–659 - ↵
Bock R (2001) Трансгенные хлоропласты в фундаментальных исследованиях и биотехнологии растений.J Mol Biol 312 : 425–438
- ↵
Bramley PM (2002) Регулирование образования каротиноидов во время созревания и развития плодов томатов. J Exp Bot 53 : 2107–2113
- ↵
Church GM, Gilbert W (1984) Геномное секвенирование. Proc Natl Acad Sci USA 81 : 1991–1995
- ↵
Collins AR (1999) Окислительное повреждение ДНК, антиоксиданты и рак.Bioessays 21 : 238–246
- ↵
Cunningham FX, Gantt E (1998) Гены и ферменты биосинтеза каротиноидов в растениях. Annu Rev Plant Physiol Plant Mol Biol 49 : 557–583
- ↵
Dharmapuri S, Rosati C, Pallara P, Aquilani R, Bouvier F, Camara B, Giuliano G (2002) Метаболическая инженерия содержания ксантофилла в плодах томатов.
 FEBS Lett 519 : 30–34
FEBS Lett 519 : 30–34 - ↵
Дойл Дж. Дж., Дойл Дж. Л. (1990) Выделение ДНК растений из свежей ткани.Фокус 12 : 13–15
- ↵
Dufourmantel N, Tissot G, Goutorbe F, Garcon F, Muhr C, Jansens S, Pelissier B, Peltier G, Dubald M (2005) Получение и анализ трансформантов пластид сои, экспрессирующих протоксин Bacillus thuringiensis Cry1Ab. Завод Мол Биол 58 : 659–668
- ↵
Fraser PD, Enfissi EMA, Halket JM, Truesdale MR, Yu D, Gerrish C, Bramley PM (2007) Манипуляция уровнями фитоена в плодах томата: влияние на изопреноиды, пластиды и промежуточный метаболизм.Растительная клетка 19 : 3194–3211
- ↵
Fraser PD, Romer S, Shipton CA, Mills PB, Kiano JW, Misawa N, Drake RG, Schuch W.
 , Bramley PM (2002) Оценка трансгенных растений томатов, экспрессирующих дополнительную фитоинсинтазу специфическим для плода образом. Proc Natl Acad Sci USA 99 : 1092–1097
, Bramley PM (2002) Оценка трансгенных растений томатов, экспрессирующих дополнительную фитоинсинтазу специфическим для плода образом. Proc Natl Acad Sci USA 99 : 1092–1097 - ↵
Galpaz N, Ronen G, Khalfa Z, Zamir D, Hirschberg J (2006) Путь биосинтеза каротиноидов, специфичный для хромопластов, обнаруживается путем клонирования локуса белого цветка томата.Растительная клетка 18 : 1947–1960
- ↵
Джулиано Г., Аквайлани Р., Дхармапури С. (2000) Метаболическая инженерия растительных каротиноидов. Trends Plant Sci 5 : 406–409
- ↵
Джулиано Дж., Тавацца Р., Директто Дж., Бейер П., Тейлор М.А. (2008) Метаболическая инженерия биосинтеза каротиноидов в растениях. Trends Biotechnol 26 : 139–145
- ↵
Hall MN, Gabay J, Debarbouille M, Schwartz M (1982) Роль вторичной структуры мРНК в контроле инициации трансляции.
 Природа 295 : 616–618
Природа 295 : 616–618 - ↵
Hirose T, Sugiura M (1997) Для трансляции мРНК ndhD хлоропласта табака необходимы как редактирование, так и расщепление РНК: возможный регуляторный механизм экспрессии оперона хлоропласта, состоящего из функционально неродственных генов. EMBO J 16 : 6804–6811
- ↵
Hirschberg J (2001) Биосинтез каротиноидов у цветковых растений.Curr Opin Plant Biol 4 : 210–218
- ↵
Isaacson T, Ronen G, Zamir D, Hirschberg J (2002) Клонирование мандарина из томатов обнаруживает каротиноид-изомеразу, необходимую для производства β -каротина и ксантофиллов в растениях. Растительная клетка 14 : 333–342
- ↵
Kahlau S, Bock R (2008) Пластидная транскриптомика и трансатомика развития плодов томатов и дифференциация хлоропластов в хромопласты: экспрессия гена хромопластов в значительной степени служит производству одного белка.
 Растительная клетка 20 : 856–874
Растительная клетка 20 : 856–874 - ↵
Kuroda H, Maliga P (2001) Комплементарность предпоследнего стебля 16S рРНК с последовательностями ниже AUG дестабилизирует пластидные мРНК. Nucleic Acids Res 29 : 970–975
- ↵
Mayer JE, Pfeiffer WH, Beyer P (2008) Биообогащенные культуры для борьбы с недостаточностью питательных микроэлементов. Curr Opin Plant Biol 11 : 166–170
- ↵
Murashige T, Skoog F (1962) Обновленная среда для быстрого роста и биологических анализов с культурой ткани табака.Physiol Plant 15 : 473–497
- ↵
Oey M, Lohse M, Kreikemeyer B, Bock R (2009) Исчерпание способности синтеза хлоропластного белка из-за массовой экспрессии высокостабильного белкового антибиотика.
 Завод J 57 : 436–445
Завод J 57 : 436–445 - ↵
Pogson B, McDonald KA, Truong M, Britton G, DellaPenna D (1996) каротиноидные мутанты Arabidopsis демонстрируют, что лютеин не важен для фотосинтеза у высших растений.Растительная клетка 8 : 1627–1639
- ↵
Römer S, Fraser PD (2005) Последние достижения в области биосинтеза, регуляции и манипулирования каротиноидами. Planta 221 : 305–308
- ↵
Römer S, Fraser PD, Kiano JW, Shipton CA, Misawa N, Schuch W., Bramley PM (2000) Повышение содержания провитамина А в трансгенных растениях томатов. Nat Biotechnol 18 : 666–669
- ↵
Ronen G, Carmel-Goren L, Zamir D, Hirschberg J (2000) Альтернативный путь образования β -каротина в хромопластах растений, обнаруженный путем клонирования на основе карт бета-мутаций и мутаций окраски старого золота в томатах.
 Proc Natl Acad Sci USA 97 : 11102–11107
Proc Natl Acad Sci USA 97 : 11102–11107 - ↵
Rosati C, Aquilani R, Dharmapuri S, Pallara P, Marusic C, Tavazza R, Bouvier F, Camara B, Giuliano G (2000) Метаболическая инженерия содержания бета-каротина и ликопина в плодах томатов. Завод J 24 : 413–419
- ↵
Ruf S, Hermann M, Berger IJ, Carrer H, Bock R (2001) Стабильная генетическая трансформация пластид томатов и экспрессия чужеродного белка во фруктах.Nat Biotechnol 19 : 870–875
- ↵
Ruf S, Karcher D, Bock R (2007) Определение уровня содержания трансгена, обеспечиваемого трансформацией хлоропластов. Proc Natl Acad Sci USA 104 : 6998–7002
- ↵
Schuetz RD, Baldwin RA (1958) Синтез и свойства некоторых замещенных фенил ω - (N, N-диалкиламино) -алкилсульфидов.
 J Am Chem Soc 80 : 162–164
J Am Chem Soc 80 : 162–164 - ↵
Svab Z, Maliga P (1993) Высокочастотная трансформация пластид в табаке путем селекции по химерному гену aadA.Proc Natl Acad Sci USA 90 : 913–917
- ↵
Wurbs D, Ruf S, Bock R (2007) Содержит метаболическую инженерию в помидорах путем экспрессии генов биосинтеза каротиноидов из пластидного генома. Завод J 49 : 276–288
- ↵
Ye X, Al-Babili S, Klöti A, Zhang J, Lucca P, Beyer P, Potrykus I (2000) Разработка пути биосинтеза провитамина A ( β -каротин) в (не содержащий каротиноидов) эндосперм риса .Наука 287 : 303–305
- ↵
Zhou F, Badillo-Corona JA, Karcher D, Gonzalez-Rabade N, Piepenburg K, Borchers A-MI, Maloney AP, Kavanagh TA, Gray JC, Bock R (2008) Высокий уровень экспрессии антигенов ВИЧ из пластидные геномы табака и томата.
 Plant Biotechnol J 6 : 897–913
Plant Biotechnol J 6 : 897–913
Диагностическая ценность аргиназы-1 и глипикана-3 в дифференциальной диагностике гепатоцеллюлярной карциномы, холангиокарциномы и метастатической карциномы печени | Гепатит Ежемесячно
Патологическое различие между различными типами опухолей печени, в основном состоящими из HCC, CC и MA, может быть очень сложной задачей, особенно при биопсии стержневой иглой (3).
Существует несколько иммуногистохимических маркеров ГЦК, включая гепатоцитоспецифический антиген (HAS или Hep Par1), альфа-фетопротеин (AFP), карциноэмбронный антиген (CEA), CD10 и CD34. К сожалению, чувствительность и специфичность этих маркеров невысоки и имеют значительные диагностические ограничения (7).
Аргиназа-1 и GLP-3 - новые иммуногистохимические маркеры, которые, как сообщается, экспрессируются при ГЦК (2). Таким образом, основной целью настоящего исследования было изучение IHC-исследования ARG-1 и GLP-3 в задокументированных случаях HCC, MA и CC.
Существует довольно много исследований, посвященных важности иммуноокрашивания ARG-1 в диагностике ГЦК. В таблице 4 обобщены результаты опубликованных исследований экспрессии ARG-1 и GLP-3 при ГЦК. Процент экспрессии ARG-1, сообщаемый в этой опухоли, колебался от 81% до 96% случаев (таблица 4). В нашем исследовании ARG-1 была продемонстрирована в 43 (100%) из 43 HCC, что было выше, чем в некоторых из предыдущих исследований. В нашем исследовании GLP-3 также экспрессируется в 42 (97.7%) ГЦК, это почти аналогично предыдущим исследованиям (8). Этот результат согласуется с предыдущим наблюдением, которое показало положительный уровень GLP-3 в диапазоне от 49% до 97% при ГЦК (таблица 4).
Таблица 4. Предыдущие исследования экспрессии аргиназы-1 и глипикана-3 при ГЦК в сравнении с текущим исследованием a, b| Исследования | Аргиназа-1 | Глипикан-3 | Тип образца | ||||||
|---|---|---|---|---|---|---|---|---|---|
| n | Положительные случаи | n | Положительные случаи 914med19 914 914 914 914 1 ) | 50 | 42 (84) | - | - | Целые разделы | |
Zaakook et al. ( 9 ) ( 9 ) | - | - | 42 | 40 (95,2) | Клеточный блок FNA | ||||
| Yan et al. ( 10 ) | - | - | 757 | 492 (65) | Целые разделы | ||||
| Anatelli et al. ( 11 ) | - | - | 74 | 36 (49) | Целые разделы | ||||
| Kring et al.( 12 ) | 160 | 151 (94) | 172 | 121 (70) | Целые разделы | ||||
| Shirakawa et al. ( 13 ) | - | - | 46 | 36 (78) | Целые разделы | ||||
| Shafizadeh et al. ( 14 ) | - | - | 58 | 46 (79) | Целые разделы | ||||
| Wang et al.( 7 ) | - | - | 111 | 84 (75,7) | Целые разделы | ||||
| Wang et al. ( 15 ) | - | - | 54 | 38 (70) | Тканевый микрочип | ||||
| Yamauchi et al. ( 6 ) | - | - | 56 | 47 (84) | Целые разделы | ||||
| Sang et al.( 2 ) | 78 | 75 (96,1) | - | - | Целые разделы | ||||
| Ян и др. ( 16 ) | 151 | 145 (96) | - | - | Тканевый микрочип | ||||
| McKnight et al. ( 17 ) | 44 | 37 (84) | 44 | 25 (57) | Блок клеток FNA | ||||
| Timek et al.( 18 ) | 29 | 23 (79) | 29 | 25 (86) | Блок клеток FNA | ||||
| Fujiwara et al. ( 19 ) | 37 | 30 (81) | 37 | 20 (54) | Блок клеток FNA | ||||
| Ибрагим и др. ( 8 ) | - | - | 30 | 29 (97) | Клеточный блок FNA | ||||
| Текущее исследование | 43 | 43 (100) | 97.7) | Целые секции | |||||
a Сокращения: FNA, Тонкоигольная аспирация.
b Данные представлены как № (%).
Среди негепатоцеллюлярных опухолей ARG-1 оказался отрицательным в 21 (77,8%) из 27 аденокарцином. Этот результат показывает статистически значимое различие между экспрессией ARG-1 при ГЦК и МА. Fujiwara et al. продемонстрировали иммунореактивность к ARG-1 в 6 (10%) из 61 общего случая аденокарциномы с помощью тонкоигольного аспирационного материала, который показал, что иммунореактивность может быть идентифицирована при аденокарциномах, особенно панкреатического происхождения (19).В исследовании Radwan и Ahmed (1) в одном случае аденокарциномы поджелудочной железы из 38 (2,6%) случаев МА, ARG-1 был положительным (1).
Хотя количество доступных исследований экспрессии GLP-3 в целых срезах негепатоцеллюлярных опухолей ограничено, в литературе позитивность GLP-3 в случаях МА варьировалась от 0 (0%) до 16,7% в материале FNA (8, 17- 19). Глипикан-3 был обнаружен в 3 из 50 случаев МА в исследовании Yan et al. по целым разделам (16). По нашим данным, 24 (88,9%) из 27 случаев МА были отрицательными по GLP-3, как и в исследовании Zaakook et al.(9), которые обнаружили, что GPC-3 был отрицательным в 83,3% случаев МА. Экспрессия в CC описана, но встречается редко. По нашим данным, только один (5,3%) и 2 (10,5%) из 19 случаев СС имели положительное окрашивание на GLP-3 и ARG-1 соответственно, что этот результат подтверждает другие исследования (таблицы 5 и 6).
Таблица 5. показывает предыдущие исследования экспрессии аргиназы-1 и глипикана-3 в негепатоцеллюлярных опухолях (метастатический AC) a| Исследования | Аргиназа-1 | Глипикан-3 | Тип образца | ||||||
|---|---|---|---|---|---|---|---|---|---|
| n | Положительные случаи | n | Положительные случаи 914med19 914 914 914 914 1 ) | 38 | 1 (2.6) | - | - | Целые разделы | |
| Zaakook et al. ( 9 ) | - | - | 18 | 3 (16,7) | Клеточный блок FNA | ||||
| Yan et al. ( 10 ) | - | - | 50 | 3 (6) | Целые разделы | ||||
| Yamauchi et al. ( 6 ) | - | - | 23 | 1 (4.34) | Целые разделы | ||||
| Sang et al. ( 2 ) | 34 | 0 (0) | Целые разделы | ||||||
| Ян и др. ( 16 ) | 99 | 0 (0) | - | - | Тканевый микрочип | ||||
| McKnight et al. ( 17 ) | 35 | 0 (0) | 35 | 0 (0) | Блок клеток FNA | ||||
| Timek et al.( 18 ) | 28 | 0 (0) | 28 | 3 (10,7) | Блок клеток FNA | ||||
| Fujiwara et al. ( 19 ) | 61 | 6 (10) | 61 | 5 (8) | Блок клеток FNA | ||||
| Ибрагим и др. ( 8 ) | - | - | 18 | 0 (0) | Клеточный блок FNA | ||||
| Текущее исследование | 27 | 6 (22.2) | 27 | 3 (11,1) | Весь раздел | ||||
a Данные представлены как № (%).
Таблица 6. Предыдущие исследования экспрессии аргиназы-1 и глипикана-3 в негепатоцеллюлярных опухолях (CC) в сравнении с текущим исследованием a| Исследования | Аргиназа-1 | Глипикан-3 | Тип образца | ||||||
|---|---|---|---|---|---|---|---|---|---|
| n | Положительные случаи | n | Положительные случаи 914med19 914 914 914 914 1 ) | 12 | 1 (8.3) | - | - | Целые разделы | |
| Yan et al. ( 10 ) | - | - | 99 | 2 (2.3) | Целые разделы | ||||
| Kring et al. ( 12 ) | 16 | 0 (0) | 16 | 1 (6) | Целые разделы | ||||
| Shirakawa et al. ( 13 ) | - | - | 28 | 0 (0) | Целые разделы | ||||
| Wang et al.( 7 ) | - | - | 10 | 1 (10) | Тканевый микрочип | ||||
| Yamauchi et al. ( 6 ) | - | - | 16 | 0 (0) | Целые разделы | ||||
| Yan et al. ( 16 ) | 6 | 1 (16,6) | - | - | Микроматрица тканей | ||||
| Timek et al.( 18 ) | 11 | 0 (0) | 11 | 0 (0) | Блок ячеек FNA | ||||
| Текущее исследование | 19 | 2 (1014,5) | 91441 (5,3) | Целые разделы | |||||
a Данные представлены как № (%).
В нашем исследовании чувствительность GPC-3 в диагностике ГЦК составила 97,7%, специфичность 91,3%, PPV 91,3% и NPV 97,7%. Эти результаты аналогичны результатам Ibrahim et al.(8), которые в своем исследовании показали, что чувствительность GPC-3 при ГЦК составила 96,7%, специфичность - 100%, PPV - 100% и NPV - 94,7%. В исследовании Timek et al. (18) чувствительность GPC-3 составила 83%, специфичность 96,7%, но Fujiwara et al. (19) показали более низкую чувствительность GPC-3, которая составила 54%, специфичность 92%, PPV 80% и NPV 77%.
В этом исследовании чувствительность ARG-1 в диагностике ГЦК составила 100%, специфичность - 82%, PPV - 84,3% и NPV - 100%. Эти результаты почти аналогичны результатам предыдущих исследований.Sang et al. (2) сообщили, что чувствительность составила 96,1%, специфичность 99,6%, PPV 98,7% и NPV 98,8%. Макнайт и др. (17) обнаружили, что чувствительность ARG-1 в различении HCC от других злокачественных новообразований, не связанных с HCC, составила 84,1%, специфичность 92,2%, PPV 74% и NPV 83,3%. Радван и Ахмед (1) обнаружили, что чувствительность составила 84%, специфичность 96%, PPV 95,5% и NPV 85,7%. В исследовании Fujiwara et al. (19) чувствительность ARG-1 составила 81%, специфичность 90%, PPV 83% и NPV 89%.
В заключение, наши результаты показывают высокую частоту положительного окрашивания на ARG-1 и GLP-3 при HCC, что они являются полезными диагностическими иммуномаркерами для отличия HCC от CC и MA.
(PDF) Глипикан-3 как новая молекулярная мишень для генной терапии гепатоцеллюлярной карциномы
Благодарности Эта работа была частично поддержана грантами от
Специальных программ медицинских наук провинции Цзянсу
(BL2012053, HK201102), Наньтун Предприятия и технологии
Инновации (HS2012039), Фонды постдокторов (2013 M53139, JS2012-
468), Китайский национальный фонд естественных наук (№ 81200634) и
Программа международного сотрудничества в области науки и технологий (2013DFA32150) Китая .
Раскрытие финансовой информации Не разглашается.
Конфликты интересов Нет
Источники
1. Тан Ю.Х., Вэнь Т.Ф., Чен Х. Предел резекции при гепатэктомии для
гепато-клеточная карцинома: систематический обзор.
Гепатогастроэнтерология. 2012. 59 (117): 1393–7. PMID: 22683956.
2. Melloul E, Lesurtel M, Carr BI, Clavien PA. Изменения в печени
Трансплантация гепатоцеллюлярной карциномы. Семин Онкол.
2012; 39 (4): 510–21.PMID: 22846868.
3. Шен Ю.С., Хсу Ц., Ченг С.К., Ху ФК, ЧенгАЛ. Критическая оценка
профилактического эффекта противовирусной терапии на развитие гепатоцеллюлярной карциномы
у пациентов с хроническим гепатитом C или B: новый подход
с использованием мета-регрессии. Онкология. 2012; 82 (5):
275–89. PMID: 22555181.
4. Wu Q, Liu Q. Увеличивают ли коинфекции вируса гепатита B и вируса гепатита C
возникновение гепатоцеллюлярной карциномы посредством синергетического
модулирования экспрессии липогенных генов? Hepatol Res.2012; 42 (8):
733–40. PMID: 22487144.
5. Эль Тази М., Эссади I, М’рабти Х., Туяр А., Эррихани PH. Системное лечение и таргетная терапия
у пациентов с распространенной гепатоцеллюлярной карциномой. N Am J Med Sci. 2011; 3 (4): 167–75. PMID: 22540086.
6. Цао Х, Фан Х, Ян Л. Улучшенная химиотерапия гепатоцеллюлярной карциномы
. Anticancer Res. 2012. 32 (4): 1379–86. PMID: 22493374.
7. Zhang HJ, Yao DF, Yao M, Huang H, Wang L, Yan MJ и др.
Подавление ANXA2 эффектов инвазии клеток MHCC97-H и моригенного потенциала tu-
. Мир J Gastroenterol. 2013. 19 (24): 3792–801.
PMID: 23840117.
8. Capurro MI, Xiang YY, Lobe C, Filmus J. Глипикан-3 способствует росту гепатоцеллюлярной карциномы
путем стимуляции канонической передачи сигналов Wnt
. Cancer Res. 2005. 65 (14): 6245–54. PMID: 16024626.
9. Цянь Дж., Яо Д., Донг З., Ву В., Цю Л., Яо Н. и др. Характеристики экспрессии
igf-ii в печени и отслеживаемые уровни циркулирующей мРНК igf-ii
при метастазах гепатоцеллюлярной карциномы.Am J Clin Pathol.
2010; 134 (5): 799–806. PMID: 20959664.
10. Донг З.З., Яо Д.Ф., Ву В., Яо М., Ю Х. Б., Шен Дж. Дж. И др. Задержка гепатоканцерогенеза
посредством антиангиогенного вмешательства в путь активации ядерного фактора
каппа B у крыс. Гепатобилиарный
Pancreat Dis Int. 2010. 9 (2): 169–74. PMID: 20382589.
11. Яо М., Яо Д.Ф., Биан Ю.З., Чжан К.Г., Цю Л.В., Ву В. и др.
Онкофетальный антиген глипикан-3 как перспективный ранний диагностический маркер
гепатоцеллюлярной карциномы.Гепатобилиарный панкреат Dis Int.
2011; 10 (3): 289–94. PMID: 21669573.
12. Биан Й.З., Яо Д.Ф., Чжан К.Г., Ли С.С., Ву В., Донг З.З. и др.
Особенности экспрессии глипикана-3 и его диагностические и дифференциальные значения
при гепатоцеллюлярной карциноме. Чжунхуа Ган Занг Бинг За
Чжи. 2011. 19 (4): 260–5. PMID: 21586223.
13. Кандил Д.Х., Купер К. Глипикан-3: новый диагностический маркер для гепатоклеточной карциномы
,и других. Adv Anat Pathol.2009; 16 (2):
125–9. PMID: 19550373.
14. Яо М., Яо Д.Ф., Биан Ю.З., Ву В., Янь XD, Ю Д.Д. и др. Значения
циркулирующихмРНК GPC-3 и AFP при обнаружении пациентов с гепа-
клеточной карциномой. Hepatobliary Pancreat Dis Int. 2013; 12 (2): 171–
9. PMID: 23558072.
15. Панг Р.В., Пун Р.Т. От молекулярной биологии до таргетной терапии
гепатоцеллюлярной карциномы: будущее уже наступило. Онкология. 2007; 72 (S1):
30–44.PMID: 18087180.
16. Капурро М.И., Ши В., Сандал С., Фильмус Дж. Обработка конвертазами не требуется
для индуцированной глипиканом-3 стимуляции роста гепатоцеллюлярной карциномы
. J Biol Chem. 2005. 280 (50): 41201–6. PMID: 16227623.
17. Зиттерманн С.И., Капурро М.И., Ши В., Фильмус Дж. Растворимый глипикан 3
подавляет рост гепатоцеллюлярной карциномы in vitro и in vivo.
Int J Cancer. 2010. 126 (6): 1291–301. PMID: 19816934.
18.Yu DD, Dong ZZ, Yao M, Wu W, Yan MJ, Yan XD и др. Нацеленная транскрипция гена
глипикана-3 ингибировала пролиферацию клеток гепатомы человека
с помощью специфической короткой шпилечной РНК. Tumor Biol.
2013; 34 (2): 661–8. PMID: 23192642.
19. Фильмус Дж., Капурро М. Роль глипикана-3 в регуляции размера и рака тела
. Клеточный цикл. 2008. 7 (18): 2787–90. PMID: 18787398.
20. Хюинь Х. Молекулярно-направленная терапия гепатоцеллюлярной карциномы.
Biochem Pharmacol. 2010. 80 (5): 550–60. PMID: 20371362.
21. Finn RS. Разработка молекулярно-направленных методов лечения клеточной карциномы гепато-
: куда нам теперь идти? Clin Cancer Res.
2010; 16 (2): 390–7. PMID: 20068087.
22. Ханахан Д., Вайнберг РА. Признаки рака: следующее поколение.
Ячейка. 2010. 144 (5): 646–74. PMID: 21376230.
23. Wysocki PJ. Таргетная терапия гепатоцеллюлярного рака. Мнение эксперта
Исследовать наркотики.2010. 19 (2): 265–74. PMID: 20074016.
24. О’Бейрн Дж., Фарзане Ф., Харрисон П.М. Генерация функциональных
CD8 + Т-клеток дендритными клетками человека, экспрессирующими топы глипикан-3 epi-
. J Exp Clin Cancer Res. 2010; 29 (1): 48. PMID: 20465843.
25. Де Кат Б., Мюлдерманс С.Ю., Куманс С., Дегест Г.,
Вандершуерен Б., Кримерс Дж. И др. Процессинг пропротеином
конвертаз необходим для модуляции глипиканом-3 выживаемости клеток, передачи сигналов
Wnt и движений гаструляции.J Cell Biol.
2003; 163 (3): 625–35. PMID: 14610063.
26. Ван Дж., Хэ XD, Яо Н., Лян В.Дж., Чжан Ю.С. Метаанализ адъювантной терапии
после потенциально излечивающего лечения гепатоцеллюлярной карциномы
. Можно J Гастроэнтерол. 2013. 27 (6): 351–63. PMID: 23781519.
27. Яо Н, Яо Д., Ван Л., Дун З., Ву В., Цю Л. и др. Ингибирование
аутокринного IGF-II на эффект пролиферации клеток HepG2 человека и экспрессию фактора ангиогенеза
.Tumor Biol. 2012; 33 (5): 1767–76.
PMID: 22684773.
28. Ли С., Яо Д., Ван Л., Ву В., Цю Л., Яо М. и др. Экспрессия
характеристика индуцируемого гипоксией фактора-1α и его клинические значения
в диагностике и прогнозе гепатоцеллюлярной карциномы. Hepat Mon.
2011; 11 (10): 821–8. PMID: 22224081.
29. Сиракава Х., Сузуки Х., Шимомура М., Кодзима М., Готода Н.,
Такахаши С. и др. Экспрессия глипикана-3 коррелирует с плохим прогнозом
при гепатоцеллюлярной карциноме.Cancer Sci. 2009; 100 (8):
1403–7. PMID: 19496787.
30. Бертино Дж., Ардири А., Малагуарнера М, Малагуарнера Дж., Бертино Н.,
Кальваньо Г.С. Сывороточные маркеры гепатоцеллюлярной карциномы. Семин
Онкол. 2012. 39 (4): 410–33. PMID: 22846859.
31. Zhuang PY, Shen J, Zhu XD, Lu L, Wang L, Tang ZY и др.
Прогностическая роль перекрестного взаимодействия между перитуморальными гепатоцитами и
стромальными клетками в гепатоклеточной карциноме с участием перитуморальных
VEGF-C, VEGFR-1 и VEGFR-3.

 Некоторые продукты могут плохо смешиваться с лекарствами или другими натуральными продуктами.
Некоторые продукты могут плохо смешиваться с лекарствами или другими натуральными продуктами. Немедленно сходите в скорую.
Немедленно сходите в скорую.


 1104/pp.109.140533
1104/pp.109.140533 Annu Rev Microbiol 51 : 629–659
Annu Rev Microbiol 51 : 629–659  FEBS Lett 519 : 30–34
FEBS Lett 519 : 30–34  , Bramley PM (2002) Оценка трансгенных растений томатов, экспрессирующих дополнительную фитоинсинтазу специфическим для плода образом. Proc Natl Acad Sci USA 99 : 1092–1097
, Bramley PM (2002) Оценка трансгенных растений томатов, экспрессирующих дополнительную фитоинсинтазу специфическим для плода образом. Proc Natl Acad Sci USA 99 : 1092–1097  Природа 295 : 616–618
Природа 295 : 616–618  Растительная клетка 20 : 856–874
Растительная клетка 20 : 856–874  Завод J 57 : 436–445
Завод J 57 : 436–445  Proc Natl Acad Sci USA 97 : 11102–11107
Proc Natl Acad Sci USA 97 : 11102–11107  J Am Chem Soc 80 : 162–164
J Am Chem Soc 80 : 162–164  Plant Biotechnol J 6 : 897–913
Plant Biotechnol J 6 : 897–913